题目内容
13.有一种混合气体,是由H2、CO、CO2、N2和HCl中的一种或几种组成,将此混合气体通入澄清的石灰水中,未见浑浊,但气体总体积明显减少;再将剩余气体在氧气中燃烧,燃烧产物不能使无水硫酸铜变蓝.则原混合气体中一定含有CO、HCl,可能含有N2、CO2.分析 根据氯化氢会与氢氧化钙反应,二氧化碳会使澄清石灰水变浑浊,无水硫酸铜遇水变蓝,氢气和一氧化碳具有可燃性等知识进行解答.
解答 解:①根据:氯化氢会与氢氧化钙发生中和反应而无明显现象,二氧化碳能使澄清石灰水变浑浊,而混合气通过澄清石灰水后,无沉淀但气体体积明显减少,可以确定混合气体中一定有氯化氢气体,可能含有二氧化碳;
②剩余的气体在氧气中燃烧,燃烧产物不能使无水硫酸铜变蓝,说明气体中不含氢元素,则一定无氢气,而含有一氧化碳.
③而氮气无法判定,可能含有.
故答案为:CO、HCl;N2、CO2.
点评 本考点考查了常见气体的检验方法,同学们要能利用物质的性质或特性来确定混合物中的成分,则应注意在学习过程中多积累有关物质检验的方法

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
3.自来水消毒过程中常会发生甲、乙两个化学反应,反应的微观过程可用下图表示:
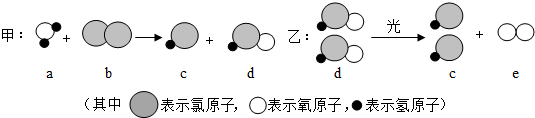
下列说法正确的是( )

下列说法正确的是( )
| A. | 物质a、b、c 分别是氧化物、单质和酸 | |
| B. | 气体b 能用排水法收集 | |
| C. | 甲、乙两反应中各有一种元素的化合价发生改变 | |
| D. | 气体e 具有可燃性 |
4.由于在重大火灾中燃烧塑料造成的二次污染、二恶英问题的出现,而且塑料燃烧过程中产生的酸性及腐蚀性气体(SO2、NO2、CO2等)的危害较大,迫使塑料工业转向使用无毒、无公害、抑烟的无机阻燃剂〔特别是Mg(OH)2和Al(OH)3〕,而占市场份额较大的溴系阻燃剂逐渐受到限制.溴系阻燃剂是目前世界上产量最大的阻燃剂,主要品种之一“八溴醚”的化学式为C21H19O2Br8.1997年在美国召开了第八届世界阻燃剂会议,会议指出今后阻燃剂的发展方向集中为高效、低毒、低烟的阻燃剂.下列有关阻燃剂说法不正确的是( )
| A. | Mg(OH)2和Al(OH)3受热分解生成气态水,可覆盖火焰,驱逐O2,稀释可燃气体 | |
| B. | Mg(OH)2和Al(OH)3受热生成的氧化物可吸收塑料燃烧过程中产生的酸性及腐蚀性气体 | |
| C. | 八溴醚是一种有机阻燃剂 | |
| D. | 有机阻燃剂使用时不可能造成环境污染 |
1. (1)实验室常用盐酸和石灰石反应制取二氧化碳.将反应后的气体通入石灰水中,有时会有在开始一段时间内未发现石灰水变浑浊的现象,其原因可能是因为浓盐酸具有挥发性,所以用浓盐酸和碳酸钙制取二氧化碳时,生成的二氧化碳中会含有氯化氢气体,将气体通入石灰水时,氯化氢溶于水形成盐酸,会将二氧化碳和石灰水反应生成的碳酸钙沉淀溶解.
(1)实验室常用盐酸和石灰石反应制取二氧化碳.将反应后的气体通入石灰水中,有时会有在开始一段时间内未发现石灰水变浑浊的现象,其原因可能是因为浓盐酸具有挥发性,所以用浓盐酸和碳酸钙制取二氧化碳时,生成的二氧化碳中会含有氯化氢气体,将气体通入石灰水时,氯化氢溶于水形成盐酸,会将二氧化碳和石灰水反应生成的碳酸钙沉淀溶解.
(2)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行.某研究小组进行了如下实验:
该实验的目的是为了研究增大反应物的接触面积可以使反应加快.
(3)另一小组也进行了同类研究,用如图所示方法成功制得了大量 CO2(反应物为稀硫酸和石灰石).
①当稀硫酸和石灰石反应,在硫酸溶液中加入的氯化铵和对溶液 加热,其目的都是增大硫酸钙在溶液中的溶解能力.
②改进实验是为了收到更好的实验效果,按上图的方法,你认为相比用盐酸和石灰石反应,其改进的出发点是证明利用稀硫酸和石灰石也可以制取二氧化碳.
 (1)实验室常用盐酸和石灰石反应制取二氧化碳.将反应后的气体通入石灰水中,有时会有在开始一段时间内未发现石灰水变浑浊的现象,其原因可能是因为浓盐酸具有挥发性,所以用浓盐酸和碳酸钙制取二氧化碳时,生成的二氧化碳中会含有氯化氢气体,将气体通入石灰水时,氯化氢溶于水形成盐酸,会将二氧化碳和石灰水反应生成的碳酸钙沉淀溶解.
(1)实验室常用盐酸和石灰石反应制取二氧化碳.将反应后的气体通入石灰水中,有时会有在开始一段时间内未发现石灰水变浑浊的现象,其原因可能是因为浓盐酸具有挥发性,所以用浓盐酸和碳酸钙制取二氧化碳时,生成的二氧化碳中会含有氯化氢气体,将气体通入石灰水时,氯化氢溶于水形成盐酸,会将二氧化碳和石灰水反应生成的碳酸钙沉淀溶解.(2)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行.某研究小组进行了如下实验:
| 试管编号 | A | B |
| 试管内药品 | 1g块状大理石与5mL25%稀硫酸 | 1g粉末状大理石与5mL25%稀硫酸 |
| 现象和比较 | 有少量气泡 | 迅速产生较多气泡 |
(3)另一小组也进行了同类研究,用如图所示方法成功制得了大量 CO2(反应物为稀硫酸和石灰石).
①当稀硫酸和石灰石反应,在硫酸溶液中加入的氯化铵和对溶液 加热,其目的都是增大硫酸钙在溶液中的溶解能力.
②改进实验是为了收到更好的实验效果,按上图的方法,你认为相比用盐酸和石灰石反应,其改进的出发点是证明利用稀硫酸和石灰石也可以制取二氧化碳.
8.金属冶炼就是把化合态变成游离态的过程,为了得到金属单质,某兴趣小组成员设想利用H2把自然界中CuO和Fe2O3混合物中的Cu和Fe冶炼出来,取100克该混合物,其中氧的质量分数为16%,用H2充分反应后最多能得H2O的质量是( )
| A. | 16克 | B. | 9克 | C. | 36克 | D. | 18克 |
19.下列有关物质用途的叙述中,不正确的是( )
| A. | 氧气用于填充食品包装 | B. | 氧气用于急救病人 | ||
| C. | 氮气可用作保护气 | D. | 稀有气体可制成多种用途的电光源 |
20.现有①液态氧;②空气;③石灰水;④冰水;⑤高锰酸钾;⑥石灰石.对物质的分类全部正确的是( )
| A. | 混合物:②③⑥ | B. | 纯净物:④⑤⑥ | C. | 单质:①④ | D. | 化合物:③⑤ |
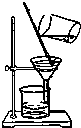 如图为过滤操作,请回答下列问题:
如图为过滤操作,请回答下列问题: