题目内容
12.请用化学方程式表示下列反应的原理:(1)水通电分解;
(2)铁和硫酸铜溶液反应;
(3)铁丝在氧气中燃烧.
分析 电解水生成氢气和氧气;
铁和硫酸铜反应生成硫酸亚铁和铜;
铁在氧气中燃烧生成四氧化三铁.
解答 解:(1)水通电分解的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)铁和硫酸铜溶液反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
(3)铁丝在氧气中燃烧的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;Fe+CuSO4═FeSO4+Cu;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
相关题目
2.现有50mL pH=9的溶液,若想使其pH=3,应加入下列哪种溶液( )
| A. | pH=0的溶液 | B. | pH=7的溶液 | C. | pH=14的溶液 | D. | pH=3的溶液 |
20.用分子的观点对下列现象的解释不正确的是( )
| A. | 氧气被压缩装入钢瓶--分子间有间隔 | |
| B. | 轮胎充气--分子间有间隔 | |
| C. | 闻到路边怡人的花香--分子不停地运动 | |
| D. | 氧气液化--分子大小发生变化 |
17.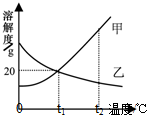 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)
甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)
 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)
甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)| A. | 随着温度的升高,甲的溶解度增大,乙的溶解度减小 | |
| B. | t1℃时,30g甲加入到50g水中最多可得80g溶液 | |
| C. | t2℃,等质量的甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液质量的大小关系为:甲<乙 | |
| D. | t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲>乙 |
4.实验室保存下列物质,不需要密封保存的是( )
| A. | 浓硫酸 | B. | 氢氧化钠 | C. | 石灰石 | D. | 浓盐酸 |
1.在反应H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O中,铜元素的化合价由+2变为0,氢元素的化合价由0变为+1.这类在化学反应前后有化合价改变的反应属于氧化还原反应.据此判断,下列反应不属于氧化还原反应的是( )
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | AgNO3+KCl═AgCl↓+KNO3 | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
13.小明用量筒量取液体时,将量筒平放,倒入液体,第一次仰视凹液面最低处,读数为18mL;倒出部分液体后,又俯视凹液面最低处,读数为10mL,则他倒出的液体体积是( )
| A. | 8mL | B. | 大于8mL | C. | 小于8mL | D. | 无法判断 |