题目内容
2.乐乐同学在盛有氧化钠的溶液的烧杯中,滴入2-3滴的酚酞试液,然后用胶头滴管吸取0.4%的稀盐酸逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边用玻璃棒搅拌,在整个实验的过程中,还利用了pH数学传感器对酸碱混合发生中和反应后溶液的pH发生变化情况进行实时监测,实验数据记录如表:| 盐酸(V/mL) | 0 | 5 | 10 | 15 | 17 | 18 | 19 | 20 | 25 | 30 |
| 溶液pH | 13.0 | 12.7 | 12.5 | 12.0 | 10.5 | 7.0 | 4.0 | 2.0 | 1.5 | 1.4 |
(1)当滴入盐酸的体积为18,此时溶液的pH=7.0,说明酸碱恰好完全反应.酸碱发生中和反应的实质是氢离子和氢氧根离子结合成水.
(2)酚酞试液变色情况如表:那么,当所得溶液变成无色的时候,你认为此溶液存在状况的所有猜想:
| pH | <8.2 | 8.2-10.0 | >10.0 |
| 显色 | 无色 | 红色 | 无色 |
②任选上述一种,在不用指示剂的情况下,实验验证该猜想正确的方法及原理是:酸性,取反应后的溶液,滴加碳酸钠溶液,有气泡产生,说明溶液显酸性.
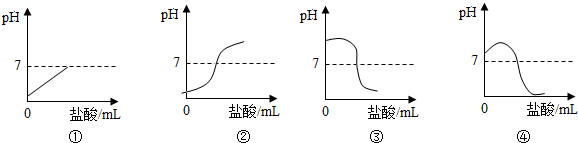
分析 (1)根据表中数据的变化情况,以及酸碱中和反应的实质进行分析;
(2)根据表中的pH值和溶液的显色范围进行分析;
根据酸会与活泼金属、碳酸盐反应进行分析.
解答 解:(1)由表可知,加入盐酸的体积是18mL时,溶液pH值是7,所以此时酸碱恰好完全反应,酸碱发生中和反应的实质是:氢离子和氢氧根离子结合成水;
(2)①当溶液的pH值小于8.2,大于10时,酚酞都显示无色,所以当所得溶液变成无色的时候,溶液显酸性、碱性、中性;
②验证猜想的方法是:酸性,取反应后的溶液,滴加碳酸钠溶液,有气泡产生,说明溶液显酸性.
故答案为:(1)18,酸碱恰好完全反应,氢离子和氢氧根离子结合成水;
(2)①酸性、碱性、中性;
②酸性,取反应后的溶液,滴加碳酸钠溶液,有气泡产生,说明溶液显酸性.
点评 本题主要考查了化学方程式的书写及其根据实验现象判断溶液的酸碱性方面的内容,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
9.在A+3B═2C+2D的反应中,7gA和24gB恰好完全反应生成C和D,若B和D的相对分子质量之比为16:9,则生成C的质量为( )
| A. | 16g | B. | 22g | C. | 44g | D. | 88g |
11.对分子、原子的认识,正确的是( )
| A. | 原子能构成分子,但不能直接构成物质 | |
| B. | 分子由原子构成,原子不能再分 | |
| C. | 分子是保持物质化学性质的一种微粒 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
12. 某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)镁条完全燃烧后,小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律,我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①通过查阅资料,记录了下列几种物质的颜色:
②镁条在氮气中也能燃烧.
【做出猜想】黄色固体是Mg3N2
【实验探究】请你设计实验方案,验证猜想:将镁条放在纯净的氮中点燃,产生黄色固体,证明产物是氮化镁.
【反思与交流】①小华同学认为,在查阅资料时,有一种物质完全可以不用考虑,请推断该物质是氯化镁(填名称),你的理由是空气中不含氯元素;
②写出镁条与氮气反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
③空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼.
 某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)镁条完全燃烧后,小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律,我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①通过查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 |
| 颜色 | 白色 | 白色 | 淡黄色 |
【做出猜想】黄色固体是Mg3N2
【实验探究】请你设计实验方案,验证猜想:将镁条放在纯净的氮中点燃,产生黄色固体,证明产物是氮化镁.
【反思与交流】①小华同学认为,在查阅资料时,有一种物质完全可以不用考虑,请推断该物质是氯化镁(填名称),你的理由是空气中不含氯元素;
②写出镁条与氮气反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
③空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼.
 实验室利用如图所示实验装置进行有关的化学实验,回答下列问题.
实验室利用如图所示实验装置进行有关的化学实验,回答下列问题.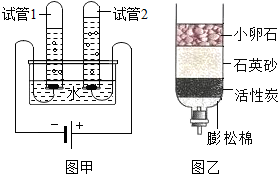 水是生命之源,人类的日常生活与工农业生产都离不开水.
水是生命之源,人类的日常生活与工农业生产都离不开水. 如图所示,打开分液漏斗,使其中的无色液体与烧瓶中的固体接触反应,可观察到尖嘴导管口处有水喷出,请分别写出一个符合图中现象和下列要求的化学方程式:
如图所示,打开分液漏斗,使其中的无色液体与烧瓶中的固体接触反应,可观察到尖嘴导管口处有水喷出,请分别写出一个符合图中现象和下列要求的化学方程式: