题目内容
6.为了除去一瓶部分变质的NaOH溶液中的Na2CO3,大家采用了不同的方法.【方案设计】:
(1)小明认为可用CaCl2溶液除去Na2CO3,大家一致认为不可行,理由是引进了新杂质氯化钠;
(2)小梁取少量部分变质的NaOH溶液于试管中,加入一定量的Ca(OH)2溶液,充分反应后,过滤,得到NaOH溶液和滤渣.加入Ca(OH)2溶液后,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【提出问题】:小明对小梁所得NaOH溶液中的溶质成分提出了疑问,认为可能仍有其他成分.
【猜想与假设】:下列是小明提出的几种滤液溶质成分的猜想:
猜想一:加入的Ca(OH)2适量,溶质只有NaOH
猜想二:加入的Ca(OH)2不足,溶质有NaOH和Na2CO3;
猜想三:加入的Ca(OH)2过量,溶质有NaOH和Ca(OH)2
【实验与探究】:分别取少量滤液于两只试管中,进行下列实验.
| 实验组别 | ① | ② |
实验操作 | 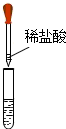 | 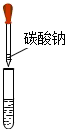 |
| 实验现象 | 无气泡产生 | 无白色沉淀产生 |
【拓展与迁移】:除了NaOH和Ca(OH)2等碱类物质,还有许多化学药品易与空气中的成分反应而变质,请再写出一例生石灰.
分析 【方案设计】(1)考虑CaCl2溶液与Na2CO3反应生成碳酸钙沉淀和氯化钠,引进了新杂质氯化钠;
(2)考虑Ca(OH)2溶液与碳酸钠反应生成碳酸钙和氢氧化钠,进行书写化学方程式.
【猜想与假设】根据反应物的量,进行推测溶质;
【实验与探究】分别取少量滤液于两只试管中,进行下列实验.根据反应物的种类进行分析;
【拓展与迁移】除了NaOH和Ca(OH)2等碱类物质,还有许多化学药品易与空气中的成分反应而变质,如生石灰、氢氧化钡等.
解答 解:
【方案设计】(1)小明认为可用CaCl2溶液除去Na2CO3,因为CaCl2溶液与Na2CO3反应生成碳酸钙沉淀和氯化钠,其化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓;故大家一致认为不可行,理由是引进了新杂质氯化钠;
(2)小梁取少量部分变质的NaOH溶液于试管中,加入一定量的Ca(OH)2溶液,充分反应后,过滤,得到NaOH溶液和滤渣.加入Ca(OH)2溶液后,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【提出问题】小明对小梁所得NaOH溶液中的溶质成分提出了疑问,认为可能仍有其他成分.
【猜想与假设】下列是小明提出的几种滤液溶质成分的猜想,根据氢氧化钙的量多少,则:
猜想一:加入的Ca(OH)2适量,溶质只有NaOH;猜想二:加入的Ca(OH)2不足,溶质有NaOH和 Na2CO3;猜想三:加入的Ca(OH)2过量,溶质有NaOH和Ca(OH)2;
【实验与探究】分别取少量滤液于两只试管中,如图进行下列实验:①滴入稀盐酸,则无气泡产生;②滴入碳酸钠溶液,无白色沉淀产生;
【事实与结论】通过以上实验探究,得出猜想 一成立.
【拓展与迁移】除了NaOH和Ca(OH)2等碱类物质,还有许多化学药品易与空气中的成分反应而变质,请再写出一例生石灰(氢氧化钡等).
故答案为:
【方案设计】(1)引进了新杂质氯化钠;(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【猜想与假设】猜想二:Na2CO3;【实验与探究】①气泡;【事实与结论】一.【拓展与迁移】生石灰.
点评 此题考查氢氧化钠溶液进行实验探究的过程,各环节层层相连,设计丝丝相扣,解题的关键是把握在证明氢氧化钠部分变质时,先除去氢氧化钠中的碳酸钠,然后再证明剩余溶液显碱性,才能说明氢氧化钠部分变质.

| 化学符号 | (1)2N2 | 3H | (3)NO3- | 氧化铜中铜元素化合价 |
| 符号的意义 | 2个氮分子 | (2)3个氢原子 | 硝酸根离子 | (4)$\stackrel{+2}{Cu}$O |
| A. | 镁条燃烧后质量增加,不遵守质量守恒定律 | |
| B. | 5g硫和5g氧气完全反应后,生成物质量为10g,遵守质量守恒定律 | |
| C. | 5g水和5g酒精混合后,总质量为10g,遵守质量守恒定律 | |
| D. | 化学反应前后分子总数一定不会发生变化 |
| A. | 挥发性 | B. | 溶解性 | C. | 可燃性 | D. | 导电性 |
| A. |  读取液体体积 | B. | 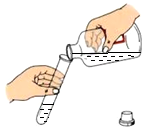 倾倒液体 | C. | 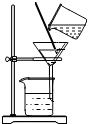 过滤 | D. |  制取二氧化碳 |
| A. | 细铁丝在氧气里剧烈燃烧,火星四射 | |
| B. | 一氧化碳燃烧产生淡蓝色火焰 | |
| C. | 二氧化碳气体通入无色酚酞溶液,溶液变红色 | |
| D. | 白磷在空气中自燃产生大量白烟 |