题目内容
11.化学实验是科学探究的重要途径.请根据下列实验图示回答相关问题: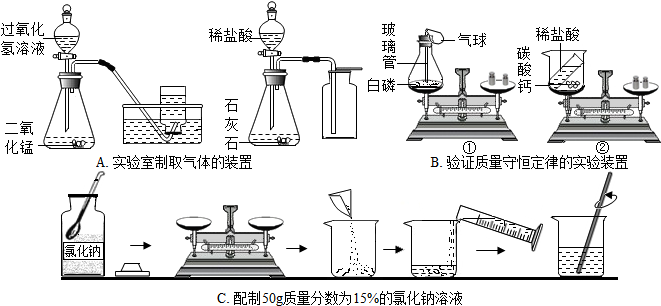
(1)A是实验室制备气体的发生于收集装置.用过氧化氢溶液与二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,制取氧气、二氧化碳可用同样的发生装置,原因是都是液体和固体在常温下反应.
(2)B实验中设计合理的是①(填“①”或“②”),另一装置设计中存在的问题是装置不密封,生成的二氧化碳扩散到空气中,没有称量计入反应后的总质量.
(3)C是定量实验,选择仪器不恰当或操作不规范都会导致实验结果有误差.实验时选择量筒规格应为50mL(填“50mL”或“100mL”),称量时砝码与药品放反了(1g以下为游码),所得溶液的质量分数小于15%(填“小于”、“等于”或“大于”).
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;根据反应物状态、反应条件可以选择发生装置;
(2)只有科学地设计实验、进行实验,才能够得出正确的结论;
(3)选择量筒时,量程应该大于或等于量取的液体体积,并且应该和量取的液体体积最接近;如果操作不当,会影响实验结果,甚至会导致实验失败.
解答 解:(1)用过氧化氢溶液与二氧化锰制取氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;制取氧气、二氧化碳可用同样的发生装置,原因是都是液体和固体反应,不需要加热;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;都是液体和固体在常温下反应.
(2)B实验中设计合理的是①,能够验证质量守恒定律;设计不合理的是②,因为装置不密封,生成的二氧化碳扩散到空气中,没有称量计入反应后的总质量,无法验证质量守恒定律.
故填:①;装置不密封,生成的二氧化碳扩散到空气中,没有称量计入反应后的总质量.
(3)50g溶液中氯化钠的质量为:50g×15%=7.5g,
水的质量为:50g-7.5g=42.5g,需要量取的水的体积为:42.5g/(1g/mL)=42.5mL,实验时选择量筒规格应为50mL;
称量时砝码与药品位置放反了,则称量的氯化钠质量为:7g-0.5g=6.5g,
所得溶液的质量分数为:$\frac{6.5g}{42.5g+6.5g}$×100%=13.3%<15%,
故填:50mL;小于.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
6.对化学变化中“变”与“不变”的描述正确的是( )
| A. | 催化剂在化学反应前后质量和性质都不变 | |
| B. | 浓硫酸稀释后溶液pH变小 | |
| C. | 复分解反应中元素的化合价一定不变 | |
| D. | 用水灭火时降低了可燃物的着火点 |
16.文明卫生城市是一项长效机制.因此,我们在日常生活中不宜提倡的是( )
| A. | 回收废旧电池 | B. | 将废报纸回收再利用 | ||
| C. | 使用一次性木筷 | D. | 减少煤炭燃料的使用 |

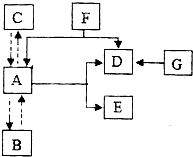 如图所示.A、B、C是水循环的三种自然状态.A为密度最大时的状态.D具有助燃性和氧化性.能与许多物质发生剧烈地、或缓慢地氧化反应.G是白色固体,加热时分解生成D和另一种固体.图中“→”表示物质间A存在转化关系;反应条件、部分反应物和生成物已略去.试回答下列问题.
如图所示.A、B、C是水循环的三种自然状态.A为密度最大时的状态.D具有助燃性和氧化性.能与许多物质发生剧烈地、或缓慢地氧化反应.G是白色固体,加热时分解生成D和另一种固体.图中“→”表示物质间A存在转化关系;反应条件、部分反应物和生成物已略去.试回答下列问题.