题目内容
1.通过化学学习,我们认识了“酸”和“碱”,请回答下列问题:(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在相同的H+(填符号),因此,它们有很多相似的化学性质,如:能使紫色石蕊试液变红,使无色酚酞试液不变色、能与碱发生中和反应等(写两条即可).
(2)碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,但不能干燥二氧化碳理由是氢氧化钠能与二氧化碳反应,氢氧化钙可由生石灰与水反应制得,反应的化学方程式为CaO+H2O=Ca(OH)2.
(3)酸和碱能发生中和反应,它在日常生活和工农业生产中有广泛的应用,如硫酸厂的污水中含有硫酸等杂质,可用熟石灰进行处理,反应的化学方程式为H2SO4+Ca(OH)2=CaSO4↓+2H2O.
(4)2010年4月14日青海玉树大地震灾害发生后,为了灾区人民群众的饮用水安全,卫生防疫部门要经常对灾区水源进行监测,获得可靠的科学依据.若现有一瓶水样,要获取它的酸碱度,应如何操作:取下一条pH试纸,用玻璃棒或胶头滴管取少量待测液,滴在试纸上,等一会与标准比色卡对比,然后读出pH的值.
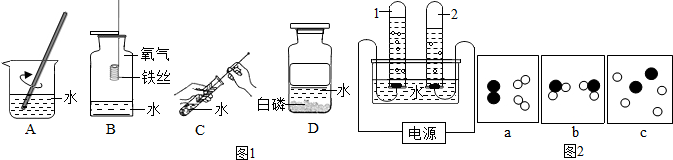
(5)某化学兴趣小组经过一段时间的调查与探究,模拟工厂的治污原理,设计了如图所示装置,一方排出含硫酸的废水,另一方排出含氢氧化钠的废水,然后在池中混合,经充分反应后排放.若该工厂一天排出含氢氧化钠10%的废液400吨,需含硫酸9.8%的废水多少吨才能完全中和?

分析 (1)理解酸的定义:酸是在水溶液中电离出的阳离子全部是氢离子的化合物.熟记酸的通性.
(2)知道碱性干燥剂只能用来干燥碱性或中性的气体.
(3)利用酸和碱能发生中和反应除杂,同时要考虑氢氧化钙经济且易得,而且生成的硫酸钙微溶于水易于除去.
(4)测定溶液酸碱度最简单的做法是采用PH试纸进行检验.
(5)利用化学方程式,根据氢氧化钠的质量求出硫酸的质量.
解答 解:(1)①因为酸是在水溶液中电离出的阳离子全部是氢离子的化合物,所以酸在水溶液中具有相同的H+,故填H+;
②回忆酸的通性可知:能使紫色石蕊试液变红,使无色酚酞试液不变色;能与碱发生中和反应;能与较活泼金属反应;能和金属氧化物反应;能和部分盐反应等;
(2)氢氧化钠等属于碱,不能用来干燥酸性的气体如二氧化碳和二氧化硫等,因为碱能与之反应;氢氧化钙可由生石灰与水反应制得,反应的化学方程式为:CaO+H2O=Ca(OH)2;
故填:氢氧化钠能与二氧化碳反应;CaO+H2O=Ca(OH)2;
(3)熟石灰成分(Ca(OH)2)属于碱,H2SO4是酸,酸碱中和反应生成盐(CaSO4)和水(H2O),正确写出反应物、生成物的化学式,再将方程式配平即可.
故反应方程式为:H2SO4+Ca(OH)2=CaSO4↓+2H2O;
(4)取下一条pH试纸,用玻璃棒或胶头滴管取少量待测液,滴在试纸上,等一会与标准比色卡对比,然后读出pH的值;
故填:取下一条pH试纸,用玻璃棒或胶头滴管取少量待测液,滴在试纸上,等一会与标准比色卡对比,然后读出pH的值;
(5)设需含硫酸9.8%的废水的质量为x
H2SO4+2NaOH═Na2SO4+2H2O
98 80
x•98% 400t×10%
$\frac{98}{80}=\frac{x•98%}{400t×10%}$
x=50t
答:需含硫酸9.8%的废水的质量为50t.
点评 本题考查酸的通性,气体的干燥,除杂,酸、碱、盐的溶解性.要求学生要熟记酸的通性、酸、碱、盐的溶解性.

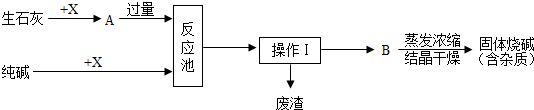
| A. | 在实验室操作Ⅰ的名称是溶解 | |
| B. | 经操作Ⅰ得到废渣的主要成份是大理石 | |
| C. | 物质X中各元素的质量比表示为1:1 | |
| D. | 若不计损失,理论上106g的纯碱可制得80g烧碱 |
| A. | ①②③④ | B. | ①④③② | C. | ④③②① | D. | ④①③② |
| A. 化学与生活 | B. 化学与健康 |
| ①热水瓶水垢可用食盐水除去 ②用燃烧方法区分棉纤维和羊毛纤维 | ③人体缺乏维生素C 易患坏血病 ④海鲜防腐可用甲醛溶液浸泡 |
| C.化学与安全 | D.化学与环境 |
| ⑤进入深井前做灯火实验 ⑥在室内放一盆水防止煤气中毒 | ⑦使用无磷洗衣粉可减少水污染 ⑧使用可降解塑料可减少“白色污染” |
| A. | A | B. | B | C. | C | D. | D |

 如图表示一瓶氯化锌溶液,请用正确的化学用语填空:
如图表示一瓶氯化锌溶液,请用正确的化学用语填空: