题目内容
3.尿素是一种高效化肥,其化学式为CO(NH2)2.试计算:(1)尿素的相对分子质量60.
(2)尿素中氮元素的质量分数46.7%.
(3)若要配制质量分数为8%的尿素溶液200g用于实验,则需要尿素多少克?同时需要水多少毫升?
分析 (1)根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(3)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
解答 解:(1)尿素的相对分子质量为12+16+(14+1×2)×2=60.
(2)尿素中氮元素的质量分数为$\frac{14×2}{60}×$100%≈46.7%.
(3)溶质质量=溶液质量×溶质的质量分数,配制质量分数为8%的尿素溶液200g,需尿素的质量=200g×8%=16g;溶剂质量=溶液质量-溶质质量,则所需水的质量=200g-16g=184g(合184mL).
故答案为:(1)60;(2)46.7%;(3)16;184.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算、溶质质量=溶液质量×溶质的质量分数等进行分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | 生活中可以通过将水煮沸来降低水的硬度 | |
| B. | 炒菜时油锅着火,立即用水浇灭 | |
| C. | 食用甲醛浸泡过的海产品,可提高人体的免疫力 | |
| D. | 用煤火取暖时,在火炉旁放一杯水以防止CO中毒 |
18. 2013年3月,浙江大学实验室诞生了世界上最年轻的材料--碳海绵.碳海绵具备高弹性和疏松多孔的结构,主要成分是石墨烯和纳米管(两者都是单质).检测结果显示碳海绵还具有超强储电能力,对有机溶剂具有超快,超高的吸附力,是已报道的吸油力最高得材料;它能达到最小密度0.16毫克、立方厘米.下例说法不正确的是( )
2013年3月,浙江大学实验室诞生了世界上最年轻的材料--碳海绵.碳海绵具备高弹性和疏松多孔的结构,主要成分是石墨烯和纳米管(两者都是单质).检测结果显示碳海绵还具有超强储电能力,对有机溶剂具有超快,超高的吸附力,是已报道的吸油力最高得材料;它能达到最小密度0.16毫克、立方厘米.下例说法不正确的是( )
 2013年3月,浙江大学实验室诞生了世界上最年轻的材料--碳海绵.碳海绵具备高弹性和疏松多孔的结构,主要成分是石墨烯和纳米管(两者都是单质).检测结果显示碳海绵还具有超强储电能力,对有机溶剂具有超快,超高的吸附力,是已报道的吸油力最高得材料;它能达到最小密度0.16毫克、立方厘米.下例说法不正确的是( )
2013年3月,浙江大学实验室诞生了世界上最年轻的材料--碳海绵.碳海绵具备高弹性和疏松多孔的结构,主要成分是石墨烯和纳米管(两者都是单质).检测结果显示碳海绵还具有超强储电能力,对有机溶剂具有超快,超高的吸附力,是已报道的吸油力最高得材料;它能达到最小密度0.16毫克、立方厘米.下例说法不正确的是( )| A. | 将来手机电池带电时间能充分满足人们的需求 | |
| B. | 若海上发生漏油事件,可以把碳海绵撒在海面上迅速吸油 | |
| C. | 碳海绵在一定条件下可以还原金属氧化物 | |
| D. | 相同体积碳海绵质量小于密度为0.09千克/立方米氢气的质量 |
13.水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)水是常用的溶剂.下表是氯化铵和氯化钠在不同温度下的溶解度.
①氯化钠常用于制0.9%的生理盐水,生理盐水中的溶质为氯化钠;
②现将180g 10%的氯化钠溶液配成为0.9%的生理盐水,需要加入蒸馏水1820g.
③40℃时,向两个分别盛有45g NH4Cl和NaCl的烧杯中,各加入100g 水,充分溶解后,结果如图1所示.则乙烧杯中的溶质是氯化铵;
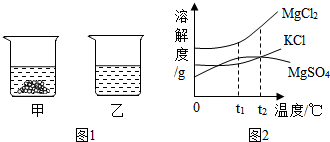
④下列有关甲、乙两烧杯的说法中,正确的是AD(填字母序号).
A.烧杯乙中溶液是不饱和溶液
B.烧杯甲中溶液溶质的质量分数为45%
C.升高温度或增加溶剂都有可能将烧杯甲中固体全部溶解
D.若将烧杯乙中溶液降温至20℃时,溶液中溶质的质量分数一定减小
(2)去除粗盐中难溶性的杂质,主要实验步骤有:溶解、过滤、蒸发.在过滤操作中,玻璃棒的作用是引流;在蒸发操作中,玻璃棒的作用是搅拌,防止局部过热造成液滴飞溅.
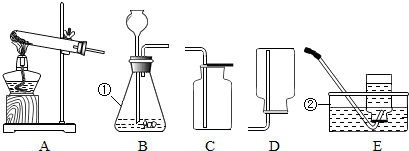
(3)晒盐场经常利用晾晒海水得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图2.将t1℃时3种物质的饱和溶液升温到t2℃时,3种溶液溶质的质量分数由小到大的顺序是KCl溶液、MgSO4溶液、MgCl2溶液.
(1)水是常用的溶剂.下表是氯化铵和氯化钠在不同温度下的溶解度.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g | NaCl | 35.7 | 36.0 | 36.6 | 37.3] | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
②现将180g 10%的氯化钠溶液配成为0.9%的生理盐水,需要加入蒸馏水1820g.
③40℃时,向两个分别盛有45g NH4Cl和NaCl的烧杯中,各加入100g 水,充分溶解后,结果如图1所示.则乙烧杯中的溶质是氯化铵;

④下列有关甲、乙两烧杯的说法中,正确的是AD(填字母序号).
A.烧杯乙中溶液是不饱和溶液
B.烧杯甲中溶液溶质的质量分数为45%
C.升高温度或增加溶剂都有可能将烧杯甲中固体全部溶解
D.若将烧杯乙中溶液降温至20℃时,溶液中溶质的质量分数一定减小
(2)去除粗盐中难溶性的杂质,主要实验步骤有:溶解、过滤、蒸发.在过滤操作中,玻璃棒的作用是引流;在蒸发操作中,玻璃棒的作用是搅拌,防止局部过热造成液滴飞溅.
(3)晒盐场经常利用晾晒海水得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图2.将t1℃时3种物质的饱和溶液升温到t2℃时,3种溶液溶质的质量分数由小到大的顺序是KCl溶液、MgSO4溶液、MgCl2溶液.
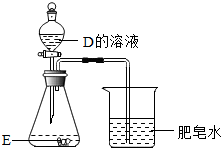 下列字母 A--H 表示初中化学常见的物质,它们由氢、碳、氧、氯、钠、钙、铁中的 2-3 种元素组成.
下列字母 A--H 表示初中化学常见的物质,它们由氢、碳、氧、氯、钠、钙、铁中的 2-3 种元素组成.