题目内容
6.【题干】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有气泡产生,反应的化学方程式是Mg+2HCl═MgCl2+H2↑.【发现问题】为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀.
【实验验证1】小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因.
| 试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
| 镁条长度 | 1cm | 2cm | 3cm | 4cm |
| 相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
| 沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
【追问】白色沉淀是什么物质?
【查阅资料】①20℃时,100g水中最多能溶解氯化镁54.8g.
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸.
【做出猜想】猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是Mg+2H2O=Mg(OH)2+H2↑(用化学方程式表示).
【实验验证2】将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
| 试管 | 操作 | 现象 | 结论 |
| A | 加入足量盐酸 | 没有气泡产生,白色沉淀消失 | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
| B | 加入足量水 | 白色沉淀不消失 | 猜想二不正确 |
| C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: Mg2+、Cl- |
| 继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
分析 【题干】根据镁与稀硫酸反应生成硫酸镁溶液和氢气,进行分析解答.
【得出结论】根据题意,实验方案,结合控制变量法,进行分析解答.
【得出结论】根据题意,镁能与热水反应产生一种碱和氢气,进行分析解答.
【做出猜想】A、由实验结论,猜想一不正确,但这种白色沉淀能溶于盐酸,进行分析解答.
B、根据题意,20℃时,100g水中最多能溶解氯化镁54.8g,易溶于水,结合实验结论猜想二不正确,进行分析解答.
C、
【实验验证2】根据加入适量稀硝酸,白色沉淀消失,继续滴加几滴硝酸银溶液,出现大量白色沉淀,进行分析解答.
解答 解:【题干】镁与稀硫酸反应生成硫酸镁溶液和氢气,在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有气泡产生,
反应的化学方程式是Mg+2HCl═MgCl2+H2↑
【做出猜想】由小林同学的实验,镁条长度越长,产生白色沉淀越多,则镁条与盐酸反应产生白色沉淀与镁条长度有关.
由题意,镁能与热水反应产生一种碱和氢气,即镁与热水反应生成氢氧化镁沉淀和氢气,猜想三为氢氧化镁,反应的化学方程式为:Mg+2H2O=Mg(OH)2+H2↑.
【实验验证2】A、镁与稀盐酸反应生成氯化镁和氢气,由实验结论,猜想一不正确,但这种白色沉淀能溶于盐酸,则没有气泡产生,白色沉淀消失.
B、20℃时,100g水中最多能溶解氯化镁54.8g,易溶于水,由实验结论,猜想二不正确,则加入足量水,白色沉淀不消失.
C、加入适量稀硝酸,白色沉淀消失,说明白色沉淀能与酸反应;继续滴加几滴硝酸银溶液,出现大量白色沉淀,说明生成了不溶于硝酸的白色沉淀,此沉淀应为氯化银沉淀,则原白色沉淀中含有的离子是:Mg2+、Cl-.
故答案为:【题干】气泡;Mg+2HCl═MgCl2+H2↑;
【实验验证1】镁条长度;
【得出结论】【做出猜想】Mg+2H2O=Mg(OH)2+H2↑;
【实验验证2】
| 试管 | 操作 | 现象 | 结论 |
| A | 加入足量盐酸 | 没有气泡产生,白色沉淀 消失 | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
| B | 加入足量水 | 白色沉淀 不消失 | 猜想二不正确 |
| C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是:Mg2+、Cl- |
点评 本题有一定难度,熟练掌握金属的化学性质、盐的化学性质、酸的化学性质并能灵活运用是正确解答本题的关键.

| A. | -1 | B. | +3 | C. | +5 | D. | +7 |
| A. | 3H:3个氢分子 | B. | Mg+2:+2价镁离子 | C. | Fe3+:铁离子 | D. | N2:2个氦原子 |
| A. | Cl-、NO3-、K+、Na+ | B. | HCO3-、Cl-、SO42-、Na+ | ||
| C. | SO42-、NO3-、K+、OH- | D. | NH4+、Cl-、OH-、K+ |
| A. | 体积小 | B. | 质量小 | C. | 不断运动 | D. | 有间隔 |
| A. | 镁条在氧气中燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| B. | 古代湿法炼铜:2Fe+3CuSO4═Fe2(SO4)3+3Cu | |
| C. | 用胃舒平[含Al(OH)3]治疗胃酸过多:Al(OH)3+3HCl═AlCl3+3H20 | |
| D. | 用石灰石浆处理二氧化硫:SO2+CaCO3+O2═CaSO4+CO2 |
| A. |  物质燃烧的条件 | B. |  常见金属的性质 | ||
| C. |  粗盐的初步提纯 | D. |  溶液的酸碱性 |
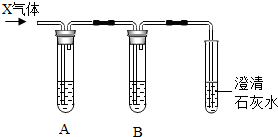 实验室用盐酸和碳酸钙固体反应,将得到的气体X通入澄淸的石灰水中,始终没有发现石灰水变浑浊,对此异常现象,同学们进行了如下探究活动:
实验室用盐酸和碳酸钙固体反应,将得到的气体X通入澄淸的石灰水中,始终没有发现石灰水变浑浊,对此异常现象,同学们进行了如下探究活动: 结合如图回答下列问题
结合如图回答下列问题