题目内容
某同学为了测定NaCl和Na2CO3固体混合物中Na2CO3的质量分数,进行如下实验:将11g固体混合物放于烧杯内,再取100g,平均分成五份,依次加入,获得如表实验数据:
问:
(1)表中m的值为 g;
(2)原固体混合物中的Na2CO3质量分数是多少?(要求写出计算过程)
(3)恰好完全反应时所得溶液 (填能或不能)作农业选种的溶液(农业上用10%的氯化钠溶液来选种)
| 实验次数 | 一 | 二 | 三 | 四 | 五 |
| 加入盐酸溶液的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 生成气体的质量(g) | 1.1 | m | 3.3 | 4.4 | 0 |
(1)表中m的值为
(2)原固体混合物中的Na2CO3质量分数是多少?(要求写出计算过程)
(3)恰好完全反应时所得溶液
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据加入20g盐酸溶液质量得到气体1.1g,第三次实验加入20g盐酸溶液生成气体增加了,说明第二次中碳酸钠还没有完全反应,所以第二次加入的20g盐酸溶液完全反应生成1.1g气体进行解答;
(2)根据图表信息可知,最终生成二氧化碳气体的质量为4.4g,利用二氧化碳的质量求出碳酸钠的质量,进而求出原固体混合物中的Na2CO3质量分数进行解答;
(3)根据二氧化碳的质量求出生成氯化钠的质量,利用溶质质量分数公式求出恰好完全反应时所得溶液的质量分数即可.
(2)根据图表信息可知,最终生成二氧化碳气体的质量为4.4g,利用二氧化碳的质量求出碳酸钠的质量,进而求出原固体混合物中的Na2CO3质量分数进行解答;
(3)根据二氧化碳的质量求出生成氯化钠的质量,利用溶质质量分数公式求出恰好完全反应时所得溶液的质量分数即可.
解答:解:(1)加入20g盐酸溶液质量得到气体1.1g,第三次实验加入20g盐酸溶液生成气体增加了,说明第二次中碳酸钠还没有完全反应,所以第二次加入的20g盐酸溶液完全反应生成1.1g气体,所以m的值为2.2;故填:2.2;
(2)根据图表信息可知,最终生成二氧化碳气体的质量为4.4g.
设样品中碳酸钠的质量分数为x,生成氯化钠的质量为y.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
=
x=10.6g
=
y=11.7g
原固体混合物中的Na2CO3质量分数=
×100%=96.4%
答:原固体混合物中的Na2CO3质量分数是96.4%.
(3)由图可知,第四次盐酸和碳酸钠恰好反应.
恰好完全反应时所得溶液的质量分数=
×100%=13.9%>10%
所以恰好完全反应时所得溶液能作农业选种的溶液.
故填:能.
(2)根据图表信息可知,最终生成二氧化碳气体的质量为4.4g.
设样品中碳酸钠的质量分数为x,生成氯化钠的质量为y.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
x=10.6g
| 117 |
| y |
| 44 |
| 4.4g |
y=11.7g
原固体混合物中的Na2CO3质量分数=
| 10.6g |
| 11g |
答:原固体混合物中的Na2CO3质量分数是96.4%.
(3)由图可知,第四次盐酸和碳酸钠恰好反应.
恰好完全反应时所得溶液的质量分数=
| 11g-10.6g+11.7g |
| 11g+20g×4-4.4g |
所以恰好完全反应时所得溶液能作农业选种的溶液.
故填:能.
点评:解答本题关键是要分析m的值时找出加入盐酸溶液的质量的关系,再推算出生成二氧化碳气体的质量.

练习册系列答案
相关题目
鉴别下列各组物质,括号中所选择的试剂或方法错误的是( )
| A、CuSO4溶液和KNO3溶液(观察颜色) |
| B、硬水和软水(过滤) |
| C、食盐和NH4NO3固体(水) |
| D、浓盐酸和蒸馏水(闻气味) |
下列物质属于纯净物的是( )
| A、液氧 | B、大理石 | C、豆浆 | D、碘酒 |
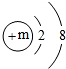 ,其微粒符号可表示为A2-,则m的值为
,其微粒符号可表示为A2-,则m的值为