题目内容
8.在CO、CO2和N2的混合气体50g,碳元素的质量分数是36%,将该混合气体与足量的灼热氧化铁完全反应,再将气体通入过量的澄清石灰水中,充分反应后得到白色沉淀的质量为( )| A. | 50g | B. | 100g | C. | 150g | D. | 200g |
分析 根据题意,在CO、CO2和N2的混合气体50g,碳元素的质量分数是36%,据此可计算出混合气体中碳元素的质量;将该混合气体与足量的灼热氧化铁完全反应,再将气体通入过量的澄清石灰水中,由质量守恒定律,碳元素最终转化为碳酸钙沉淀,据此进行分析解答.
解答 解:在CO、CO2和N2的混合气体50g,碳元素的质量分数是36%,混合气体中碳元素的质量为50g×36%=18g.
将该混合气体与足量的灼热氧化铁完全反应,一氧化碳与氧化铁反应生成铁和二氧化碳,再将气体通入过量的澄清石灰水中,二氧化碳与石灰水反应生成碳酸钙沉淀和水,由质量守恒定律,碳元素最终转化为碳酸钙沉淀,则充分反应后得到白色沉淀的质量为18g÷($\frac{12}{40+12+16×3}$×100%)=150g.
故选:C.
点评 本题难度不大,灵活运用质量守恒定律(反应前后碳元素的质量不变)是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.我国青海湖采集的天然碱样品可表示为aNa2CO3•bNaHCO3•cH2O(a、b、c为最简整数比).某实验小组为测定其组成,称取该天然碱样品16.6g进行如下实验:
资料Ⅰ:碳酸氢钠不稳定,加热易分解为碳酸钠、二氧化碳和水,而碳酸钠比较稳定,
加热时不分解;
资料Ⅱ:图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
资料Ⅲ:装置C、F、G中都是碱石灰(CaO与NaOH的固体混合物)
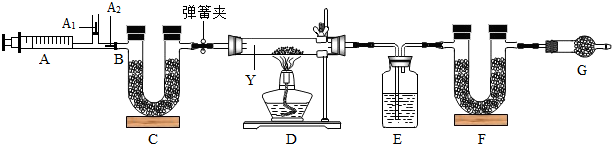
【实验步骤】①连接好装置,先检查装置的气密性;②反复推拉注射器;③称量E、F的质量;④关闭弹簧夹,加热D处试管直到反应不再进行;⑤打开弹簧夹,再次反复缓缓推拉注射器;⑥再次称量E、F的质量.
问题探究】
(1)仪器Y的名称是硬质玻璃管;
(2)实验步骤①连接好装置,先检查装置的气密性;
(3)E中的药品为浓硫酸(填名称),目的是吸收水蒸气,F的作用是吸收生成的二氧化碳,G的作用是防止空气中的二氧化碳和水蒸气被F吸收;
(4)实验步骤②与③能否颠倒不能(填“能”或“不能”). 若无装置C,则所测得的碳酸氢钠质量分数偏大(填“偏大”、“偏小”、“无影响”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使残留在装置中的二氧化碳和水蒸气充分被吸收.
(5)写出装置D中发生的化学反应化学方程式aNa2CO3•bNaHCO3•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$$\frac{2a+b}{2}$Na2CO3+$\frac{b+2c}{2}$H2O+$\frac{b}{2}$CO2↑(计量数用abc表示)
(6)通过右表数据,求得该天然碱化学式中a:b:c=2:1:2.(写出过程,4分)
资料Ⅰ:碳酸氢钠不稳定,加热易分解为碳酸钠、二氧化碳和水,而碳酸钠比较稳定,
加热时不分解;
资料Ⅱ:图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
资料Ⅲ:装置C、F、G中都是碱石灰(CaO与NaOH的固体混合物)

【实验步骤】①连接好装置,先检查装置的气密性;②反复推拉注射器;③称量E、F的质量;④关闭弹簧夹,加热D处试管直到反应不再进行;⑤打开弹簧夹,再次反复缓缓推拉注射器;⑥再次称量E、F的质量.
问题探究】
(1)仪器Y的名称是硬质玻璃管;
(2)实验步骤①连接好装置,先检查装置的气密性;
(3)E中的药品为浓硫酸(填名称),目的是吸收水蒸气,F的作用是吸收生成的二氧化碳,G的作用是防止空气中的二氧化碳和水蒸气被F吸收;
(4)实验步骤②与③能否颠倒不能(填“能”或“不能”). 若无装置C,则所测得的碳酸氢钠质量分数偏大(填“偏大”、“偏小”、“无影响”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使残留在装置中的二氧化碳和水蒸气充分被吸收.
(5)写出装置D中发生的化学反应化学方程式aNa2CO3•bNaHCO3•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$$\frac{2a+b}{2}$Na2CO3+$\frac{b+2c}{2}$H2O+$\frac{b}{2}$CO2↑(计量数用abc表示)
| 反应前 | 反应后 | |
| 装置E的质量/g | 100.0 | 102.25 |
| 装置F的质量/g | 50.0 | 51.1 |
5.雾霾是今年“两会”点击率颇高的词汇.雾霾是雾和霾的混合物,其中雾是自然天气现象,霾的核心物质是悬浮在空气中的烟、灰尘等物质.下列做法能减少雾霾的是( )
| A. | 开私家车出行 | B. | 使用太阳能热水器 | ||
| C. | 用煤火力发电 | D. | 露天焚烧垃圾 |
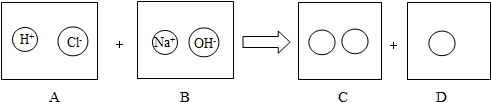
 水时生命之源.
水时生命之源.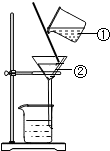 如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答: