题目内容
18.下列各组变化中,每一转化在一定条件下均能一步实现的是( )
| A. | ①和② | B. | ①和③ | C. | ②和③ | D. | ①②③ |
分析 抓住物质间反应的规律,理解复分解反应的条件:必须有水、气体或沉淀生成,及一些特殊的反应.
解答 解:①过氧化氢分解生成了水和氧气,电解水能生成氧气,每步均可以一步实现,符合题意;
②碳在充分燃烧时生成了二氧化碳,在不充分燃烧时生成了一氧化碳,一氧化碳燃烧生成了二氧化碳,每步均可以一步实现.符合题意;
③氢氧化钠与盐酸反应可生成氯化钠,氯化钠与硝酸银反应可生成硝酸钠,但硝酸钠不能通过一部反应生成氢氧化钠,不符合题意.
由以上分析可知,A正确.
故选A.
点评 主要考查了物质间的反应的规律,培养学生分析问题、解决问题的能力.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
13.下列说法不正确的是( )
| A. | 白磷在空气中燃烧会产生大量的白烟 | |
| B. | 打开盛有浓盐酸的试剂瓶盖,瓶口会出现白雾 | |
| C. | 一氧化碳通过灼热氧化铁,固体由红色变为黑色 | |
| D. | 水通电后,与正极相连的电极上产生的气体是氢气 |
3.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业.如图2、3是两种不同方法制备一水柠檬酸晶体(C6H8O7•H2O)的工艺流程图.回答相关问题:
【资料卡片】: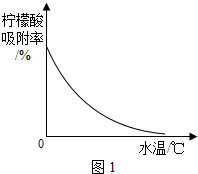
①柠檬酸水溶液显酸性,柠檬酸钙不溶于水;
②工业生产柠檬酸,原料预处理后,得到的发酵液中含有柠檬酸及其他可溶性杂质;
③一水柠檬酸在不同温度下的溶解度如下表:
④某种专用树脂对柠檬酸的吸附率和水温的关系如图1:
【钙盐法制备】(图2)
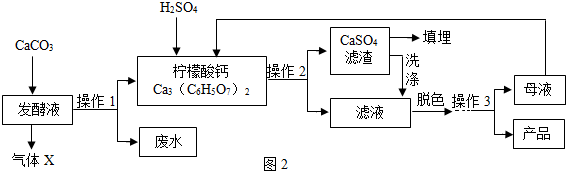
(1)实验室检验气体X时发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
(2)操作3的目的是得到一水柠檬酸晶体,操作顺序是加热浓缩→冷却结晶→过滤.
(3)洗涤CaSO4滤渣的目的是提高产量;
(4)母液可以循环,其中一定含有的溶质是柠檬酸;
【变温色谱分离法制备】(图3)
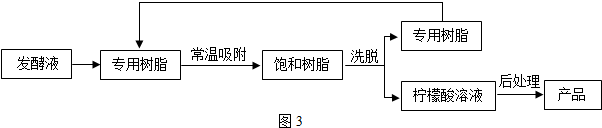
(5)洗脱的目的是使专用树脂再生,洗脱时在较高温度下的热水进行,其原因是专用树脂对柠檬酸的吸附率随温度升高而降低,温度越高,越便于柠檬酸从专用树脂中分离;
(6)对比“变温色谱分离法”,请你说出“钙盐法”的劣势钙盐法中增加了废水及CaSO4滤渣后期处理的费用;增加了CO2的排放;消耗资源,破坏环境.
【资料卡片】:

①柠檬酸水溶液显酸性,柠檬酸钙不溶于水;
②工业生产柠檬酸,原料预处理后,得到的发酵液中含有柠檬酸及其他可溶性杂质;
③一水柠檬酸在不同温度下的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | … |
| 溶解度/g | 96 | 118 | 146 | 183 | 216 | … |
【钙盐法制备】(图2)

(1)实验室检验气体X时发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
(2)操作3的目的是得到一水柠檬酸晶体,操作顺序是加热浓缩→冷却结晶→过滤.
(3)洗涤CaSO4滤渣的目的是提高产量;
(4)母液可以循环,其中一定含有的溶质是柠檬酸;
【变温色谱分离法制备】(图3)

(5)洗脱的目的是使专用树脂再生,洗脱时在较高温度下的热水进行,其原因是专用树脂对柠檬酸的吸附率随温度升高而降低,温度越高,越便于柠檬酸从专用树脂中分离;
(6)对比“变温色谱分离法”,请你说出“钙盐法”的劣势钙盐法中增加了废水及CaSO4滤渣后期处理的费用;增加了CO2的排放;消耗资源,破坏环境.
10.下列物质由原子构成的是( )
| A. | 金刚石 | B. | 氯化钠 | C. | 氢气 | D. | 蔗糖 |
7. 某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )
某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )
 某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )
某品牌碳酸氢铵化肥的标签如下图所示.根据相关信息判断下列计算正确的是( )| A. | 碳酸氢铵中氮、氢、氧、碳四种元素的质量比14:4:12:48 | |
| B. | 碳酸氢铵中各元素的质量分数由大到小的顺序为O、C、H、N | |
| C. | 该化肥中碳酸氢铵的纯度为79% | |
| D. | 每袋该化肥中含氮量与30kg尿素[化学式为CO(NH2)2]含氮量相当 |
8. 甲、乙两种物质的溶解度曲线如图所示,下列叙述正碥的是( )
甲、乙两种物质的溶解度曲线如图所示,下列叙述正碥的是( )
 甲、乙两种物质的溶解度曲线如图所示,下列叙述正碥的是( )
甲、乙两种物质的溶解度曲线如图所示,下列叙述正碥的是( )| A. | 甲的溶解度比乙的大 | |
| B. | 将甲、乙的饱和溶液从t2℃降到t1℃析出甲的质量大 | |
| C. | 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法 | |
| D. | t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等 |

 通过化学的学习,小明同学感悟到学校化学开拓了思维、增长了智慧.
通过化学的学习,小明同学感悟到学校化学开拓了思维、增长了智慧. ”代表碳原子,“○”代表氢原子.请补充该物质燃烧的化学方程式:C5H4+6O2$\frac{\underline{\;点燃\;}}{\;}$5CO2+2H2O
”代表碳原子,“○”代表氢原子.请补充该物质燃烧的化学方程式:C5H4+6O2$\frac{\underline{\;点燃\;}}{\;}$5CO2+2H2O