题目内容
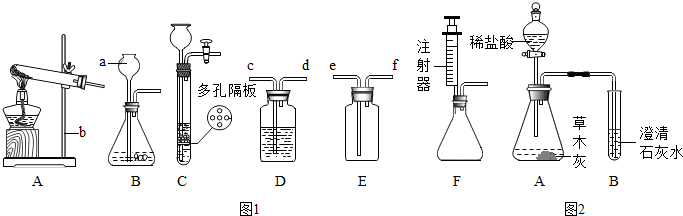
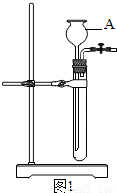
图-1是实验室制取二氧化碳气体的装置图,请回答下列问题:①写出仪器A的名称______.②检查此装置的气密性时,关闭弹簧夹,从仪器A处注入适量的______形成液封后,若看到仪器A内______,则表明装置气密性良好.
③为了制得较多的二氧化碳,可对图中所示仪器进行改变,请写出你的方法______.
④同学们在图-1装置不漏气、操作正确、加入药品足量且质量相等的情况下同时进行了实验.
以下是他们的实验记录:
| 甲 | 乙 | |
| 现象 | 产生气泡缓慢并逐渐停止. | 反应剧烈,产生气泡很快. |
经过以上实验分析,你认为影响反应速度快慢的因素有______等.
丙同学重新选择药品,进行实验并观察到产生气泡速度适中.但是将产生气体通入足量的澄清石灰水,澄清石灰水不浑浊.请你分析可能的原因:______;
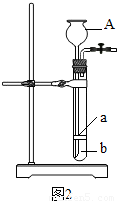
⑤同学们在图-1装置中添加了多孔隔板,得到了图-2所示装置.添加多孔隔板的作用是______. 实验过程中,将固体药品放在______(填a或b)处,从A处加入一定量液体,从而产生二氧化碳.若关闭弹簧夹,继续反应产生的二氧化碳会使容器内______,将液体压回仪器A中,使固体与液体______,反应即自行停止.
⑥请写出证明二氧化碳气体已经集满的方法______.
⑦同学们确定了合适的药品进行实验,成功收集到0.01mol二氧化碳气体.实验中消耗了10克盐酸(假设溶质全部反应完),请问该盐酸溶液溶质的质量分数?(根据化学方程式列式计算)
【答案】分析:①根据实验室常见仪器名称及用途,进行解答;
②根据检查装置的气密性的方法进行解答;
③根据题意制得较多的二氧化碳,可更换试管为较大容器;
④根据实验室制取二氧化碳的反应原理、方法、操作注意事项进行分析解答本题;
⑤根据图-2装置能将固体液体完全分离,进行解答本题;
⑥根据二氧化碳气体集满的方法进行解答;
⑦根据二氧化碳气体的量依据化学方程式计算出消耗盐酸的量,依据溶质的质量分数= ×100%,进行解答.
×100%,进行解答.
解答:解:①根据实验室常见仪器名称及用途,可知仪器A的名称为:长颈漏斗;
②根据检查装置的气密性的方法:在仪器A处注入适量的 水形成液封后,若看到仪器A内液面不下降,则表明装置气密性良好;
③根据题意制得较多的二氧化碳,可更换试管为较大容器,如:将试管换成锥形瓶或广口瓶或用启普发生器;
④根据实验室制取二氧化碳的反应原理、方法、操作注意事项,分析产生两种现象的可能的原因甲同学:使用了硫酸;乙同学:使用碳酸钙粉末(或碳酸钠);反应物的接触面积越大反应速度越快,反应物种类不反应速度不同;
因此影响反应速度快慢的因素有:反应物的接触面积等;
根据浓盐酸具有挥发性,收集到的二氧化碳不纯,澄清石灰水不浑浊;
⑤根据图-2装置能将固体液体完全分离,可知添加多孔隔板的作用是放置块状固体; 实验过程中,将固体药品放在 a 处,从A处加入一定量液体,从而产生二氧化碳.若关闭弹簧夹,继续反应产生的二氧化碳会使容器内压强增大,将液体压回仪器A中,使固体与液体分离,反应即自行停止;
⑥根据二氧化碳气体集满的方法:用燃着的木条放在瓶口,如果木条熄灭,则说明瓶内已收集满二氧化碳;
⑦设:消耗了xmolHCl
CaCO3+2HCl=CaCl2+CO2↑+H2O
2 1
x 0.01
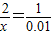 则 x=0.02mol
则 x=0.02mol
HCl的质量:0.02 mol×36.5 g/mol=0.73 g
盐酸溶质质量分数为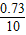 ×100%=7.3%;
×100%=7.3%;
答:消耗的盐酸溶质质量分数为7.3%.
故答案为:
①长颈漏斗(错别字扣分);
②水; 液面不下降;
③将试管换成锥形瓶或广口瓶或用启普发生器(答案合理即可)
④甲使用了硫酸;乙使用了碳酸钙粉末(碳酸钠也对,答案合理即可);反应物种类、反应物的接触面积 (本小题(2分),漏写一个扣1分);丙同学使用了浓盐酸.
⑤放置块状固体;a;压强增大;分离.
⑥用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;(方法、位置必须都正确).
⑦设:消耗了x mol HCl
CaCO3+2HCl=CaCl2+CO2↑+H2O
2 1
x 0.01
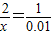 则 x=0.02mol
则 x=0.02mol
HCl的质量:0.02 mol×36.5 g/mol=0.73 g
盐酸溶质质量分数为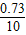 ×100%=7.3%;
×100%=7.3%;
答:消耗的盐酸溶质质量分数为7.3%
点评:本题考查学生掌握二氧化碳的反应原理、实验室制法及注意事项、化学性质检验方法及验满;根据化学方程式进行计算的解题能力.
②根据检查装置的气密性的方法进行解答;
③根据题意制得较多的二氧化碳,可更换试管为较大容器;
④根据实验室制取二氧化碳的反应原理、方法、操作注意事项进行分析解答本题;
⑤根据图-2装置能将固体液体完全分离,进行解答本题;
⑥根据二氧化碳气体集满的方法进行解答;
⑦根据二氧化碳气体的量依据化学方程式计算出消耗盐酸的量,依据溶质的质量分数=
 ×100%,进行解答.
×100%,进行解答.解答:解:①根据实验室常见仪器名称及用途,可知仪器A的名称为:长颈漏斗;
②根据检查装置的气密性的方法:在仪器A处注入适量的 水形成液封后,若看到仪器A内液面不下降,则表明装置气密性良好;
③根据题意制得较多的二氧化碳,可更换试管为较大容器,如:将试管换成锥形瓶或广口瓶或用启普发生器;
④根据实验室制取二氧化碳的反应原理、方法、操作注意事项,分析产生两种现象的可能的原因甲同学:使用了硫酸;乙同学:使用碳酸钙粉末(或碳酸钠);反应物的接触面积越大反应速度越快,反应物种类不反应速度不同;
因此影响反应速度快慢的因素有:反应物的接触面积等;
根据浓盐酸具有挥发性,收集到的二氧化碳不纯,澄清石灰水不浑浊;
⑤根据图-2装置能将固体液体完全分离,可知添加多孔隔板的作用是放置块状固体; 实验过程中,将固体药品放在 a 处,从A处加入一定量液体,从而产生二氧化碳.若关闭弹簧夹,继续反应产生的二氧化碳会使容器内压强增大,将液体压回仪器A中,使固体与液体分离,反应即自行停止;
⑥根据二氧化碳气体集满的方法:用燃着的木条放在瓶口,如果木条熄灭,则说明瓶内已收集满二氧化碳;
⑦设:消耗了xmolHCl
CaCO3+2HCl=CaCl2+CO2↑+H2O
2 1
x 0.01
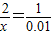 则 x=0.02mol
则 x=0.02mol HCl的质量:0.02 mol×36.5 g/mol=0.73 g
盐酸溶质质量分数为
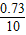 ×100%=7.3%;
×100%=7.3%;答:消耗的盐酸溶质质量分数为7.3%.
故答案为:
①长颈漏斗(错别字扣分);
②水; 液面不下降;
③将试管换成锥形瓶或广口瓶或用启普发生器(答案合理即可)
④甲使用了硫酸;乙使用了碳酸钙粉末(碳酸钠也对,答案合理即可);反应物种类、反应物的接触面积 (本小题(2分),漏写一个扣1分);丙同学使用了浓盐酸.
⑤放置块状固体;a;压强增大;分离.
⑥用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;(方法、位置必须都正确).
⑦设:消耗了x mol HCl
CaCO3+2HCl=CaCl2+CO2↑+H2O
2 1
x 0.01
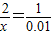 则 x=0.02mol
则 x=0.02mol HCl的质量:0.02 mol×36.5 g/mol=0.73 g
盐酸溶质质量分数为
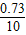 ×100%=7.3%;
×100%=7.3%;答:消耗的盐酸溶质质量分数为7.3%
点评:本题考查学生掌握二氧化碳的反应原理、实验室制法及注意事项、化学性质检验方法及验满;根据化学方程式进行计算的解题能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目