题目内容
将50g Na2CO3溶液和55g CaCl2溶液混合后,恰好完全反应,过滤,得到100g滤液.求:
(1)反应后生成沉淀的质量为______.
(2)过滤后所得溶液中溶质的质量分数.
解:(1)依据质量守恒定律可知反应后生成沉淀的质量为50g+55g-100g=5g;
(2)设反应生成的氯化钠的质量是x
CaCl2+Na2CO3=2NaCl+CaCO3↓
117 100
x 5g
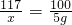
x=5.85g
故过滤后所得溶液中溶质的质量分数 ×100%=5.85%
×100%=5.85%
故答案为:(1)5g;(2)过滤后所得溶液中溶质的质量分数5.85%;
分析:依据反应前后溶液质量的变化可以求出生成的沉淀碳酸钙的质量,据此可以求出溶液中氯化钠的质量,即可解决过滤后所得溶液中溶质的质量分数.
点评:此题是对化学方程式计算的考查题,解题的关键是利用质量守恒定律求出生成的碳酸钙的质量;
(2)设反应生成的氯化钠的质量是x
CaCl2+Na2CO3=2NaCl+CaCO3↓
117 100
x 5g
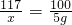
x=5.85g
故过滤后所得溶液中溶质的质量分数
 ×100%=5.85%
×100%=5.85%故答案为:(1)5g;(2)过滤后所得溶液中溶质的质量分数5.85%;
分析:依据反应前后溶液质量的变化可以求出生成的沉淀碳酸钙的质量,据此可以求出溶液中氯化钠的质量,即可解决过滤后所得溶液中溶质的质量分数.
点评:此题是对化学方程式计算的考查题,解题的关键是利用质量守恒定律求出生成的碳酸钙的质量;

练习册系列答案
相关题目
20
℃时,KCl的溶解度为34g,此温度下将50g KCl溶于70g水中,充分溶解后,所得溶液的溶质的质量分数为[ ]
|
A .71% |
B .41.7% |
|
C .25.4% |
D .50% |