题目内容
3. 化学与人类生活的关系越来越切
化学与人类生活的关系越来越切(1)如图是某种加碘食盐包装标签上的部分内容.请用化学用语表示下列带点部分:
①该食盐的主要成分是$\underset{氯化钠}{…}$NaCl;
②食用该食盐可补充$\underset{钙元素}{…}$Ca;
③碘原子的结构示意图为
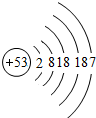 ,碘原子在化学反应中易形成$\underset{碘离子}{…}$I-.
,碘原子在化学反应中易形成$\underset{碘离子}{…}$I-.(2)下列各类物质可以作为食品干燥剂的是① (填序号,下同).
①生石灰 ②浓硫酸 ③氯化钠 ④硝酸铵
(3)下列生活中的物品,属于金属材料的是①.
①汽车外壳 ②不锈钢锅 ③棉布围裙 ④塑料保鲜盒
(4)洗涤剂能除去衣服上的油污,洗涤剂的作用是乳化.
(5)车用乙醇汽油可适当节省石油资源,并在一定程度上减少汽车尾气的污染.乙醇燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)①氯化钠是由显+1价的钠元素和显-1价的氯元素组成的,根据化合价原则,其化学式为:NaCl;
②元素可用元素符号表示,钙元素的元素符号为:Ca;
③离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.碘离子可表示为:I-;
(2)①生石灰即氧化钙,能与水生成氢氧化钙,具有很强的吸水性,无毒,可用作食品的干燥;故A正确;
②浓硫酸为一种粘稠状液体,具有较强的吸水性和腐蚀性,可用于气体的干燥,但却不能用作食品干燥剂;故B不正确;
③氯化钠不能吸收水分无干燥能力;故C不正确;
④烧碱即氢氧化钠,能吸收空气中水分而潮解,是常用的干燥剂,但由于有极强的腐蚀性,而不能用作食品干燥剂;故D不正确;
故选①
(3)①汽车外壳是合金,属于金属材料,故选项正确.
②不锈钢锅是用不锈钢制成的,不锈钢是铁的合金,属于金属材料,故选项正确.
③棉布围裙是用天然纤维制成的,真丝属于天然材料,故选项错误.
④塑料保鲜盒是用塑料制成的,塑料属于合成材料,故选项错误.
故选①
(4)洗涤剂能除去衣服上的油污,洗涤剂的作用是乳化;
(5)乙醇燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答案:(1)①NaCl;②Ca;③I-;(2)①;(3)①;(4)乳化;(5)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案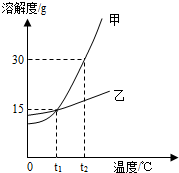 甲、乙两物质的溶解度曲线如图所示,下列说法错误的是( )
甲、乙两物质的溶解度曲线如图所示,下列说法错误的是( )| A. | t1℃时,甲、乙两物质的溶解度相等 | |
| B. | t2℃时甲和乙的饱和溶液溶质质量分数大小关系:乙>甲 | |
| C. | 0~t1℃时,甲的溶解度小于乙的溶解度 | |
| D. | 将甲的饱和溶液变为不饱和溶液,可采用升高温度的方法 |
(1)海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如图:
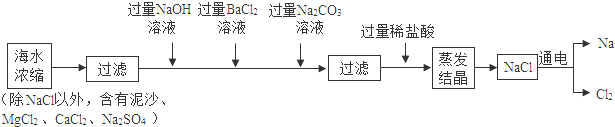
①加入过量Na2CO3溶液目的是除去CaCl2和氯化钡,流程中不能用过量稀硫酸代替过量稀盐酸的原因是会生成新的杂质硫酸钠;
②提纯过程中使用了过滤和蒸发操作,实验室过滤和蒸发操作均使用到的玻璃仪器是玻璃棒;
③流程图中制备金属钠的化学方程式为2NaCl$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑.
(2)工业上利用电解饱和食盐水的方法制备NaOH,并同时获得两种单质.补充并配平化学方程式:
□NaCl+□H2O$\frac{\underline{\;通电\;}}{\;}$□NaOH+□H2+□Cl2↑
(3)刘廷在实验室找到一瓶长期放置的NaOH溶液,欲对其成分进行实验探究.
【查阅资料】
I.NaOH与CO2分两步反应:
2NaOH+CO2═Na2CO3+H2O;Na2CO3+CO2+H2O═2NaHCO3
Ⅱ.NaOH与NaHCO3反应方程式为:NaOH+NaHCO3═Na2CO3+H2O
Ⅲ.物质的溶解性:
| CO32- | HCO3- | OH- | |
| Ba2+ | 不溶 | 溶 | 溶 |
【提出猜想】刘廷根据资料中的I、Ⅱ对其成分提出了5种合理猜想,请将猜想补充完整
猜想1:只有NaOH,猜想2:含有氢氧化钠、碳酸钠,猜想3:只有Na2CO3,猜想4:碳酸氢钠、碳酸钠,
猜想5:只有NaHCO3.
【实验验证】
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取该NaOH溶液,加入过量BaCl2溶液 | 产生白色沉淀 | 证明猜想1、5不成立(填数字) |
| 步骤2 | 取步骤1中上层清液,滴加稀盐酸 | 无气泡产生 | 证明原溶液不含HCO3-(填“离子”) |
| 步骤3 | 另取步骤1中上层清液,滴加酚酞 | 溶液未变红 | 证明原溶液不含OH-(填“离子”) |
通过以上实验操作得出结论:猜想3是正确的(填数字)
| A. | 从分类上看:葛根素属于化合物 | |
| B. | 从构成上看:葛根素由21个碳原子、20个氢原子和9个氧原子构成 | |
| C. | 从组成上看:葛根素由碳、氢、氧三种元素组成 | |
| D. | 从变化上看:葛根素完全燃烧会生成二氧化碳和水 |
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末.打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
【探究与反思】
(1)打火石是混合物(填“混合物”或“纯净物”).
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?金属被石蜡包围,无法接触到氧气.
(3)这种蜡烛也可以熄灭,你采用的方法是隔绝氧气.
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验 | 操作步骤 | 实验现象 | 实验结论 |
| 1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石是银白色 | |
| 2 | 取少量打磨后的打火石加试管中,滴加盐酸 | 该金属一定不是铁 | |
| 3 | 取少量打磨后的打火石加试管中,滴加硫酸铜溶液 | 有色物质析出 | 该金属一定是镁 |
请写出“实验3”中可能涉及到的化学方程式Mg+CuSO4=MgSO4+Cu.
| A. | X Y Z | B. | X Z Y | C. | Y X Z | D. | Z Y X |
| A. | 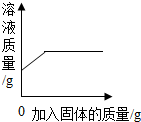 一定温度下,向饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| B. | 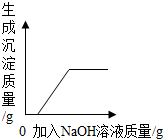 向硫酸和硫酸铜混合溶液中滴加过量的氢氧化钠溶液 | |
| C. | 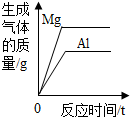 将等质量的镁粉和铝粉分别与足量等浓度的稀硫酸反应 | |
| D. | 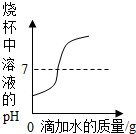 向盛有一定量稀硫酸的烧杯中不断加水稀释 |
