题目内容
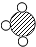
13.分子、原子和离子都是构成物质的粒子.A、B、C、D四种物质的微观示意图如图所示:| A | B | C | D |
 | 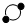 |  |  |
(1)A物质的元素符号Fe;
(2)B物质的分子式CO2;
(3)C(由离子构成)物质的化学式NaCl;
(4)D物质的分子式NH3.
分析 观察A、B、C、D四种物质的微观示意图,根据微粒的构成特点,写出符合要求的符号.
解答 解:(1)A物质是由原子直接构成,符合A物质构成的元素符号可以是Fe等;
(2)由B物质微观构成可知,符合B物质的分子式有:CO2等;
(3)C(由离子构成)物质的,离子的个数比是1:1,符合C(由离子构成)物质的构成的有氯化钠等,化学式是:NaCl;
(4)D物质的分子是由两种原子构成,原子个数比是1:3,例如氨气等符合D物质的分子构成,分子式是:NH3.
故答为:(1)Fe;(2)CO2;(3)NaCl;(4)NH3.
点评 解决这种题的关键就是辨别分子是由何种原子构成,每种原子有几个,这样就可以得出分子的化学式.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
3.鉴别下列物质所使用的试剂错误的是( )
| A. | 氧化铜粉和木炭粉--加稀硫酸 | |
| B. | 氢氧化钠溶液和碳酸钠溶液--加酚酞溶液 | |
| C. | 生石灰和石灰石--加水 | |
| D. | 氯化钠和氯化铵--加熟石灰研磨 |
4.小苏打(主要成分为NaHCO3)中常含有少量氯化钠.化学兴趣小组的同学为了测定某品牌小苏打中NaHCO3的质量分数.进行了以下实验:称量样品置于烧杯中,向其中慢慢滴加稀盐酸,至不再产生气泡为止,测得的有关数据如下表所示.
试计算:
(1)样品中NaHCO3的质量分数.
(2)反应后所得NaCl的质量.
| 物质 | 样品 | 加入稀盐酸质量 | 反应后烧杯中物质的总质量 |
| 质量(g) | 9 | 55.4 | 60 |
(1)样品中NaHCO3的质量分数.
(2)反应后所得NaCl的质量.
8. 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
【提出问题】这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是氯化钠.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
【设计实验】
[实验结论]
(3)该瓶无色溶液是碳酸钠溶液.生成白色沉淀过程的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
[实验反思]
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是向溶液中加入盐酸,碳酸钠能与盐酸反应生成二氧化碳气体,而硫酸钠不能与盐酸反应.经查阅资料得知上述五种盐中碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方案,确定该溶液究竟是哪种盐.简述实验操作和现象取溶液滴加酚酞试液,若溶液变红,则是碳酸钠溶液,若溶液不变色,则是硫酸钠溶液.
 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.【提出问题】这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是氯化钠.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
【设计实验】
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 |
(3)该瓶无色溶液是碳酸钠溶液.生成白色沉淀过程的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
[实验反思]
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是向溶液中加入盐酸,碳酸钠能与盐酸反应生成二氧化碳气体,而硫酸钠不能与盐酸反应.经查阅资料得知上述五种盐中碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方案,确定该溶液究竟是哪种盐.简述实验操作和现象取溶液滴加酚酞试液,若溶液变红,则是碳酸钠溶液,若溶液不变色,则是硫酸钠溶液.
5.“酸雨”的形成主要是由于( )
| A. | 大气中二氧化碳的含量增加 | |
| B. | 工业上大量燃烧含硫燃料 | |
| C. | 汽车排出大量尾气 | |
| D. | 森林遭到乱砍滥伐,破坏了生态环境 |
2.小明同学对部分化学知识归纳如下,其中不完全正确的一组是( )
| A | 物质使用与安全常识 | B | 元素与人体健康 |
| 点燃可燃性气体之前-检验纯度 汽车在加油站加油-严禁烟火 冬天用燃煤炉子取暖-注意通风 | 缺铁-会引起贫血 缺碘-会引起甲状腺肿大 缺锌-会引起龋齿 | ||
| C | 生活中常见物质的鉴别 | D | 环境保护与资源利用 |
| 黄铜和黄金-灼烧,观察颜色变化 棉线和羊毛绒-灼烧,闻气味 白酒和白醋-闻气味 | 减少使用塑料袋-减缓白色污染 推广使用乙醇汽油-减缓温室效应 回收利用废旧金属-节约金属资源 |
| A. | A | B. | B | C. | C | D. | D |
3.下列物质之间的转化,能通过一步反应实现的是( )
①CH4→CO2②CaCO3→Ca(OH)2③CuSO4→FeSO4④HNO3→HCl⑤Fe3O4→Fe.
①CH4→CO2②CaCO3→Ca(OH)2③CuSO4→FeSO4④HNO3→HCl⑤Fe3O4→Fe.
| A. | ①③④ | B. | ①③⑤ | C. | ①③④⑤ | D. | ①②③⑤ |
 为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中溶质成分,将废液过滤,取滤液20g于烧杯中,在不断振荡的条件下,向其中滴加溶质质量分数为10.6%的碳酸钠溶液至过量,相关变化如图所示,回答下列问题:
为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中溶质成分,将废液过滤,取滤液20g于烧杯中,在不断振荡的条件下,向其中滴加溶质质量分数为10.6%的碳酸钠溶液至过量,相关变化如图所示,回答下列问题: