题目内容
18.将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列说法正确的是( )①滤渣中一定有锌
②滤渣中一定有铜,可能有锌
③向滤渣中加入足量的稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
| A. | ②④ | B. | ①④⑤ | C. | ②③④ | D. | ②③④⑤ |
分析 根据金属活动性顺序表进行分析.在金属活动性顺序中,排在氢前面的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:由金属活动顺序表可知,金属的活动性顺序是:镁>锌>铁>铜.所以将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,首先锌粉和硫酸铜溶液反应,置换出单质铜,如果锌粉足量可以继续与硫酸亚铁反应置换出铁,不能与硫酸镁反应.由于是“一段时间后过滤“,所以不能视为完全反应.向滤出的固体中滴加稀盐酸,有气泡产生,说明固体中含有和稀盐酸反应的金属,由题可知,金属可能是铁或铁和锌还要可能就是只有锌,这种情况是加入的锌尚在和硫酸铜反应的过程中就被过滤了,由上述分析可知:
①滤渣中不一定有锌,故①说法错误;
②滤渣中一定有铜,可能有锌,故②说法正确;
③向滤渣中加入稀盐酸,根据固体的三种可能性,溶液不见得会变成浅绿色由于有铁生成,最后溶液一定变成浅绿色,故③说法不正确;
④滤液中溶质一定含有硫酸锌和硫酸镁,故说法正确;
⑤若锌的量不足,不能将硫酸亚铁全部置换出,则滤液的颜色可能为浅绿色.故⑤说法错误
综合上述分析可知,C正确.
故选C.
点评 本题主要考查了学生对金属活动顺序表的运用,在解题时要注意对半定量(如一定量、过量、少量等)概念的理解和掌握.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
8.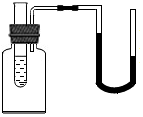 如图所示,向试管中加入某些物质后,U型管中液面出现如图所示的水位差,则加入的物质是( )
如图所示,向试管中加入某些物质后,U型管中液面出现如图所示的水位差,则加入的物质是( )
 如图所示,向试管中加入某些物质后,U型管中液面出现如图所示的水位差,则加入的物质是( )
如图所示,向试管中加入某些物质后,U型管中液面出现如图所示的水位差,则加入的物质是( )| A. | 硝酸钾固体 | B. | 硝酸铵固体 | C. | 氯化钠固体 | D. | 氢氧化钠固体 |
9.生活中下列做法不正确的是( )
| A. | 用烧碱洗去锅碗内的油污 | B. | 进入久置菜窖需做灯火实验 | ||
| C. | 用煮沸法将硬水软化 | D. | 小苏打可用于治疗胃酸过多症 |
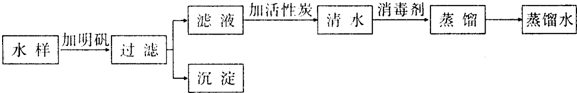

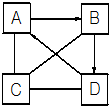 A、B、C、D是初中化学常见的四种不同类别的物质,A、B、D在一定条件下可相互转化,C与A、B、D均能发生反应,D与C发生中和反应,C还能与AgNO3溶液反应可产生不溶于稀硝酸的白色沉淀.(-表示两端的物质间能发生化学反应;→表示物质间存在转化关系;)
A、B、C、D是初中化学常见的四种不同类别的物质,A、B、D在一定条件下可相互转化,C与A、B、D均能发生反应,D与C发生中和反应,C还能与AgNO3溶液反应可产生不溶于稀硝酸的白色沉淀.(-表示两端的物质间能发生化学反应;→表示物质间存在转化关系;)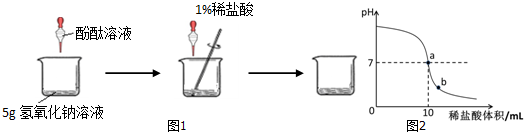
 按如图是细铁丝在氧气中燃烧的实验.
按如图是细铁丝在氧气中燃烧的实验.