题目内容
2.2003年10月,中国“神舟五号”载人飞船顺利升空,圆了中华民族的升天梦.“神舟五号”运载火箭的燃料是偏二甲肼(C2H8N2).(1)偏二甲肼的相对分子质量是60.
(2)碳、氢、氮的质量比是6:2:7.
(3)碳元素的质量分数是40%.
(3)一个青少年正常情况下每天约需0.8g钙.若每天从牛奶中得到0.6g钙,那么,他每天应补充多少g葡萄糖酸钙[(C6H11O7)2Ca]?
分析 (1)根据偏二甲肼的化学式可知,其相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)+(氮的相对原子质量×氮原子个数);
(2)偏二甲肼中碳、氢、氮的质量比=(碳的相对原子质量×碳原子个数):(氢的相对原子质量×氢原子个数):(氮的相对原子质量×氮原子个数);
(3)偏二甲肼中碳元素的质量分数=$\frac{碳的相对原子质量×碳原子个数}{偏二甲肼的相对分子质量}$×100%.
(4)根据题意,一个人正常情况下每天约需0.8g钙.如果每天从食物中得到0.6g钙,则每天从葡萄糖酸钙中补充0.2g钙,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)根据偏二甲肼的化学式可知,其相对分子质量=12×2+8+14×2=60;
(2)偏二甲肼中碳、氢、氮的质量比=(12×2):8:(14×2)=6:2:7;
(3)偏二甲肼中碳元素的质量分数=$\frac{12×2}{60}$×100%=40%.
(4)由题意,一个人正常情况下每天约需0.8g钙.如果每天从食物中得到0.6g钙,
则每天从葡萄糖酸钙中补充0.2g钙.
每天应补充葡萄糖酸钙[(C6H11O7)2Ca]的质量为0.2g÷($\frac{40}{(12×6+11+16×7)×2+40}×$100%)=2.15g
答:每天应补充葡萄糖酸钙[(C6H11O7)2Ca]2.15g.
故答案为:(1)60;
(2)6:2:7;
(3)40%;
点评 本题主要考查考查学生运用化学式和元素的质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
12.某学习小组在探究CO2与NaOH溶液反应的实验中,先用铝制易拉罐收集满一罐CO2气体,然后迅速向其中加入-定量的NaOH浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计).
(提出问题)易拉罐为什么先瘪后鼓?
(分析猜想)易拉罐开始时变瘪的原因是CO2+2NaOH═Na2CO3+H2O(用化学方程式表示),
易拉罐重新鼓起的原因是易拉罐中又生成了气体A,其成分极有可能是CO2或H2.
(查阅资料)①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;②铝单质比较容易被酸、碱腐蚀.
(设计方案并进行实验)为了检验铝制易拉罐中重新生成的气体成分,小组又进行如下实验,并记录了相应的实验现象:
[实验结论]①铝制易拉罐变瘪的原因是CO2被NaOH溶液吸收,②铝制易拉罐重新鼓起的原因是铝与NaOH溶液反应产生了气体.
[反思评价]小组根据实验探究获得一条对金属铝化学性质的新认识:铝单质既能与酸反应,又能与碱反应,均能生成氢气.
[拓展延伸]A1与NaOH溶液反应产生了气体的同时还生成另一种书写形式类似于KMnO4的盐,请完成下列反应化学方程式:2Al+2NaOH+2H2O=2NaAlO2 +3A↑.当然,本实验只是初步探究,还有进一步探究的价值,有待我们在以后的学习中去深究.
(提出问题)易拉罐为什么先瘪后鼓?
(分析猜想)易拉罐开始时变瘪的原因是CO2+2NaOH═Na2CO3+H2O(用化学方程式表示),
易拉罐重新鼓起的原因是易拉罐中又生成了气体A,其成分极有可能是CO2或H2.
(查阅资料)①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;②铝单质比较容易被酸、碱腐蚀.
(设计方案并进行实验)为了检验铝制易拉罐中重新生成的气体成分,小组又进行如下实验,并记录了相应的实验现象:
| 实验步骤 | 实验现象 | 实验结论 |
| 将易拉罐口打开,迅速用燃着的木条伸入罐口. | 发出“噗”的-声,产生淡蓝色火焰,片刻后熄灭. | 说明罐中重新生成的气体A是氢气 |
| 取少量铝片于试管中,先加入适量的水,片刻后再加入少量的氢氧化钠溶液. | 先加水,没有明显变化,后加入氢氧化钠溶液后产生无色无味的气体. | 说明铝是否与水直接反应:否( 填“是”或“否”),铝能够与NaOH溶液反应. |
| 取少量易拉罐中反应后的溶液于试管中,加入过量的稀盐酸. | 产生了无色无味气体,该气体能使澄清石灰水变浑浊. | 说明原CO2气体被NaOH溶液吸收 |
[反思评价]小组根据实验探究获得一条对金属铝化学性质的新认识:铝单质既能与酸反应,又能与碱反应,均能生成氢气.
[拓展延伸]A1与NaOH溶液反应产生了气体的同时还生成另一种书写形式类似于KMnO4的盐,请完成下列反应化学方程式:2Al+2NaOH+2H2O=2NaAlO2 +3A↑.当然,本实验只是初步探究,还有进一步探究的价值,有待我们在以后的学习中去深究.
10.关于燃烧一氧化碳:(2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2)说法正确的是( )
| A. | 反应过程中吸收大量的热 | |
| B. | 反应前后分子个数不变 | |
| C. | 参加反应的一氧化碳和氧气的质量比是:2:1 | |
| D. | 反应物的化学计量数之比是2:1 |
14.据悉,目前我国生产的配制酱油中含致癌物---氯丙醇含量严重超标,为此欧盟国家将限制中国酱油出口到欧洲市场.在酿制酱油中绝对不含氯丙醇.在氯丙醇中以三氯丙醇对人体的危害最大,其化学式为C3H5OCl3下列有关说法正确的是( )
| A. | 提倡将配制酱油与酿制酱油混合使用 | |
| B. | 三氯丙醇属于无机物 | |
| C. | 三氯丙醇的分子由12个原子构成 | |
| D. | 三氯丙醇的相对分子质量是160.5 |
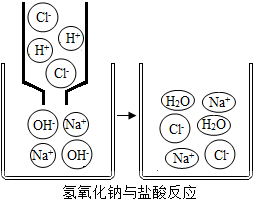 今有①肥皂水 ②食盐水 ③杨梅汁 ④白糖水 ⑤蒸馏水,5种液体,根据你的生活经验判断,其中pH<7的是③,pH>7的是①,pH=7的是②④⑤(填序号).右图是氢氧化钠与盐酸反应的微观示意图,请仔细观察、分析此图,写出一条你从图中获取的信息(用文字或化学用语表述)氢氧化钠与盐酸反应的实质是氢离子与氢氧根离子反应生成水.
今有①肥皂水 ②食盐水 ③杨梅汁 ④白糖水 ⑤蒸馏水,5种液体,根据你的生活经验判断,其中pH<7的是③,pH>7的是①,pH=7的是②④⑤(填序号).右图是氢氧化钠与盐酸反应的微观示意图,请仔细观察、分析此图,写出一条你从图中获取的信息(用文字或化学用语表述)氢氧化钠与盐酸反应的实质是氢离子与氢氧根离子反应生成水.