题目内容
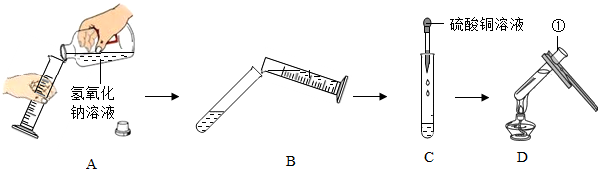
9.探究:“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”是指在NaCl中按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2). 学习小组探究某“低钠盐”中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种),设计了如下实验方案,请完成表格中的内容.| 实验操作 | 现象 | 结论 |
| 步骤1:取样品加水溶解,滴加 NaOH溶液 | 观察到有白色沉淀生成现象, | “低钠盐”加入了MgCl2 |
| 步骤2:继续向步骤1所得溶液中滴加少量BaCl2溶液 | 观察到无明显现象 |
分析 根据镁离子的验证和硫酸根的验证分析;
反思评价:根据AgNO3溶液和MgSO4反应生成硫酸银沉淀解答.
解答 解:
探究样品中是否还有镁盐,即探究是否含有Mg2+,而探究是何种镁盐就是探究是否含有SO42-.先将样品溶解,注意要加足量蒸馏水,并用玻璃棒搅拌.步骤1,验证是否含有Mg2+,可以加NaOH 溶液会产生Mg(OH)2,现象为有白色沉淀生成,说明样品b中添加了镁盐.步骤,2,因为题目说是MgSO4或MgCl2中的一种而且样品中一定还有Cl-,因此只要检测是否含有SO42-.操作:取少量步骤1 形成的溶液于试管中,再滴加少量的BaCl2溶液振荡观察.现象及结论,若有白色沉淀产生,则添加的是MgSO4.若无明显现象,则添加的是MgCl2.
反思评价:取该低钠盐样品加水溶解,滴加AgNO3溶液和稀硝酸,若有沉淀生成,则样品中添加了MgCl2.你认为该方案不合理,因为AgNO3溶液和MgSO4反应生成硫酸银沉淀,不能证明样品中添加了MgCl2.
故答案为:
| 实验操作 | 现象 | 结论 |
| 步骤1:取样品加水溶解,滴加 NaOH溶液 | 观察到 有白色沉淀生成现象, | “低钠盐”加入了MgCl2 |
| 步骤2:继续向步骤1所得溶液中滴加少量BaCl2溶液 | 观察到 无明显现象 |
点评 本题主要是考查学生对离子的验证的理解能力,同时注意语言的准确性.物质推断过程中注意加入的试剂可能对后续检验造成的干扰,所以要避免引入待鉴定的离子或者物质.

练习册系列答案
相关题目
19.我国科学家屠呦呦因为发现青蒿素(化学式为C15H22O5),而获诺贝尔奖.下列关于青蒿素的说法正确的是( )
| A. | 一个分子中含有42个原子 | |
| B. | 相对分子质量为281 | |
| C. | 氢元素的质量分数大于氧元素质量分数 | |
| D. | 碳、氢、氧元素的质量比为15:22:5 |
4.下列实验进行中的现象或实验原理正确的是( )
| A. | 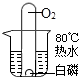 白磷始终不燃烧 | B. | 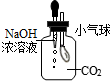 小气球变瘪 | ||
| C. | 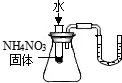 U形管内液面左高右低 | D. | 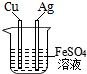 验证Fe,Cu,Ag的金属活性强弱 |
14.固体混合物A是由Mg、CuO、Na2SO4、Na2CO3、BaCl2、BaSO4中的几种混合而成,为确定其成分,进行如图实验.(假设每步反应均恰好完全反应)下面推断不正确的是( )
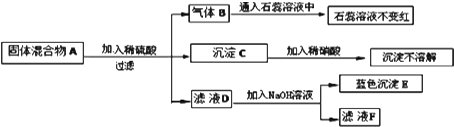

| A. | 由气体B可推原固体混合物A中一定含有Mg,一定不含Na2CO3. | |
| B. | 沉淀C一定为BaSO4,由此可推原固体混合物A中一定含有BaCl2和Na2SO4 | |
| C. | 滤液D中一定含有的溶质是MgSO4和CuSO4 | |
| D. | 固体A的组成可能有6种. |
1.成语被誉为中华民族的瑰宝.下列成语中,其本意主要为化学变化的是( )
| A. | 磨杵成针 | B. | 木已成舟 | C. | 死灰复燃 | D. | 积土成山 |
18.下列关于实验现象的描述正确的是( )
| A. | 磷在氧气中燃烧,产生大量白色烟雾 | |
| B. | 木炭在氧气中燃烧,发出白色火焰,生成使澄清石灰水变浑浊的气体 | |
| C. | 镁带在空气中燃烧,发出耀眼的白光,放出大量的热,生成白色固体 | |
| D. | 蜡烛在空气中燃烧,发白光,放出大量的热 |