题目内容
(11分)冶炼1680 t含杂质3%的生铁,需要含Fe3 04 90%的磁铁矿石多少吨?
(Fe304+4C0 3Fe+4C02;得数保留小数点后1位)
3Fe+4C02;得数保留小数点后1位)
(1)根据化学方程式计算。
(2)根据反应过程铁元素质量守恒原理计算。
【解析】
设需要含Fe3O4 90%的磁铁矿石的质量是m
(1)Fe3O4+4CO 高温 3Fe+4CO2
232 3×56
90%m 1680 t×(1-3%)
232 3×56
90%m 1680 t×(1-3%)
m =2500.4 t
(2)90%m×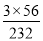 = 1680 t×(1-3%)
= 1680 t×(1-3%)
m =2500.4 t
答:需要含Fe3O4 90%的磁铁矿石的质量是2500.4 t
【解析】
试题分析:(1)方程式已知Fe3O4+4CO 高温 3Fe+4CO2;已知1680 t含杂质3%的生铁,那么该反应中铁的质量=1680 t×(1-3%);需要含Fe304 90%的磁铁矿石多少吨;通过方程式就可以求得需要的Fe304 的质量,再求得铁矿石质量;(2)即根据铁元素质量的不变;
考点:化学方程式的计算,化学式的计算

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
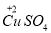 ⑤O2- ⑥H2O2
⑤O2- ⑥H2O2 2CO 化合反应
2CO 化合反应 Cu+CO2 置换反应
Cu+CO2 置换反应