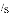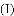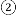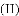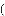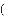题目内容
用化学用语表示
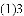
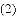
某化学探究小组用盐酸与大理石的反应来研究影响反应速率的因素。实验温度为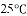
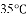
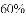
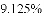
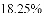

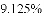
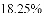
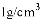 ;大理石中杂质不与盐酸反应
;大理石中杂质不与盐酸反应
(提岀假设)盐酸与大理石反应的反应速率与所用盐酸的质量分数、大理石规格、反应温度有关。
实验 编号 |
| 大理石 规格 | 盐酸的 质量分数 | 完全反应 的时间 | 实验目的 |
| 25 | 粗颗粒 |
| 160 |
|
| ______ | ______ | ______ | 210 | |
| 35 | 粗颗粒 |
| 60 | |
| ______ | ______ | ______ | 100 |

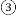
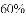
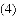
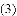
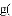
下列实验设计能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较空气和呼出气体中CO2含量 | 分别伸入燃着的木条 |
B | 鉴别真金和假金(铜锌合金) | 加入硫酸铜固体 |
C | 鉴别CO和H2 | 分别点燃,观察火焰的颜色 |
D | 鉴别铁粉和碳粉 | 空气中灼烧 |
A. A B. B C. C D. D
小科冋学阅读课外资料得知,某些氧化物可代替二氧化锰作一些反应的催化剂,于是她对此产生了探究兴趣、
(提倡问题)氧化铜能否作氯酸钾分解的催化剂?
(设计实验)小科设计了下列三组实验(其他可能影响实验的因素均忽略)
实验编号 | KC1O3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
1 | 0.6 | / | 9.8 | 480 |
2 | 0.6 | 0.2g氧化铜 | 67 | 90 |
3 | 0.6 | 0.2g二氧化锰 | 67 | 37 |
(1)写出氯酸钾用二氧化锰作催化剂的化学方程式______。
(2)从实验1与实验2的数据可知,氧化铜______(选填“能”或“不能”)加快氯酸钾的分解速率。
(3)为证明氧化铜是该反应的催化剂,小科又完成了以下的实验。
1,将实验2反应后的混合物加足量的水溶解,过滤,洗涤并十燥,用天平称量,质量为0.2g。
Ⅱ.将过量的CO通入滤出的固体,按如图进行实验,小科同学的实验报告如下表,请填写空格中的内容。
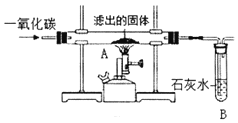
装置 | 现象 | 结论 |
A | ______ | 生成了铜 |
B | 澄清的石灰水变成浑浊 | 产生了二氧化碳 |
(得出结论)通过I、Ⅱ实验证明氧化铜能作氯酸钾分解的催化剂。
(反思与评价)
从环保角度分析,上图装置有不足之处,你认为该如何改进?______。