题目内容
 在t℃时,称量5.2g氢氧化钠,投入到15g水中搅拌,固体全部溶解.冷却到t℃后有0.2g固体析出.判断下列正确的是
在t℃时,称量5.2g氢氧化钠,投入到15g水中搅拌,固体全部溶解.冷却到t℃后有0.2g固体析出.判断下列正确的是
- A.称量5.2g氢氧化钠时用到5g和0.2g的砝码
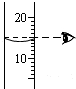
- B.用右图所示的操作方法,量取15mL的水
- C.氢氧化钠固体溶解于水时,溶液温度升高
- D.t℃时氢氧化钠的溶解度为25g
C
分析:A、根据托盘天平的使用方法进行分析判断.
B、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
C、根据氢氧化钠溶于水的温度变化进行分析判断.
D、溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量.
解答:A、称量5.2g氢氧化钠时用到5g的砝码,需将游码拨到0.2刻度处,故选项说法错误.
B、量取液体时,视线与液体的凹液面最低处保持水平,图中视线没有与液体的凹液面最低处保持水平,故选项说法错误.
C、氢氧化钠固体溶解于水时,放出大量的热,溶液温度升高,故选项说法正确.
D、在t℃时,称量5.2g氢氧化钠,投入到15g水中搅拌,冷却到t℃后有0.2g固体析出,说明该温度下,15g水中最多能溶解5g氢氧化钠,则t℃时氢氧化钠的溶解度为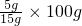 =30g,故选项说法错误.
=30g,故选项说法错误.
故选C.
点评:本题难度不大,掌握饱和溶液与不饱和溶液的特征、常见化学实验基本操作、氢氧化钠溶于水的温度变化、溶解度的概念等是正确解答本题的关键.
分析:A、根据托盘天平的使用方法进行分析判断.
B、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
C、根据氢氧化钠溶于水的温度变化进行分析判断.
D、溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量.
解答:A、称量5.2g氢氧化钠时用到5g的砝码,需将游码拨到0.2刻度处,故选项说法错误.
B、量取液体时,视线与液体的凹液面最低处保持水平,图中视线没有与液体的凹液面最低处保持水平,故选项说法错误.
C、氢氧化钠固体溶解于水时,放出大量的热,溶液温度升高,故选项说法正确.
D、在t℃时,称量5.2g氢氧化钠,投入到15g水中搅拌,冷却到t℃后有0.2g固体析出,说明该温度下,15g水中最多能溶解5g氢氧化钠,则t℃时氢氧化钠的溶解度为
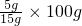 =30g,故选项说法错误.
=30g,故选项说法错误.故选C.
点评:本题难度不大,掌握饱和溶液与不饱和溶液的特征、常见化学实验基本操作、氢氧化钠溶于水的温度变化、溶解度的概念等是正确解答本题的关键.

练习册系列答案
相关题目
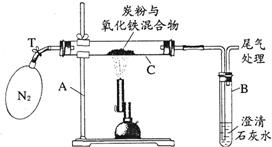
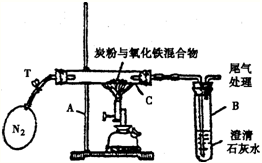 (2005?湘潭)某化学兴趣小组的学生研究过量的碳粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
(2005?湘潭)某化学兴趣小组的学生研究过量的碳粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下: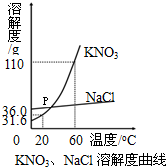
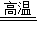 4Fe+3CO2↑ C+C02
4Fe+3CO2↑ C+C02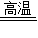 2CO
2CO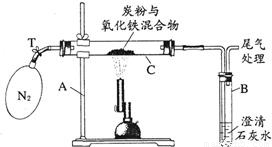
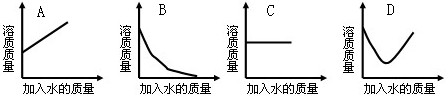
 。
。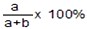 ,若要使其溶质质量分数变为原来的1/2倍,需加水_________克。
,若要使其溶质质量分数变为原来的1/2倍,需加水_________克。