题目内容
19.将一种无色无味的液体A装入试管,用带火星的木条试验,无明显现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属D红热并伸入盛有气体C中,瓶底有少量水的集气瓶中,金属D剧烈燃烧,火星四射,生成黑色固体E.(1)写出各物质的名称:
A:过氧化氢,C:氧气;
(2)黑色粉末B在该反应中起催化作用;
(3)写出金属D在C中燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
分析 根据C“使带火星的木条复燃”,故C为氧气,无色无味的液体A中加入少量黑色粉末B后,迅速产生氧气,根据氧气的制法可知A为双氧水,B为二氧化锰;金属D在氧气中剧烈燃烧,火星四射,生成黑色固体E,则D为铁,E为四氧化三铁;据此完成相关的问题.
解答 解:根据题目中的信息可知:C使带火星的木条复燃,故C为氧气,无色无味的液体A中加入少量黑色粉末B后,迅速产生氧气,根据氧气的制法可知A为双氧水,B为二氧化锰;金属D在氧气中剧烈燃烧,火星四射,生成黑色固体E,则D为铁,E为四氧化三铁;由上述分析可知A为过氧化氢,B为二氧化锰,C为氧气,D为铁,E为四氧化三铁;因此:
(1)A为过氧化氢,C为氧气;故答案为:过氧化氢;氧气;
(2)B为二氧化锰,在过氧化氢分解中起到催化作用;故填:催化;
(3)铁和氧气点燃产生四氧化三铁,故化学反应方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 本题属于常见物质的推断题,解题关键是根据物质的物理性质或明显的化学反应特征,找准解题的突破口,并从突破口出发结合物质间的关系得出结论,带入验证符合要求即可.

练习册系列答案
相关题目
9. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t1℃时,甲物质50g加入到100g水中,充分溶解,得到的溶液质量都是150g | |
| C. | t1℃时,甲的饱和溶液的溶质质量分数等于乙饱和溶液的溶质质量分数 | |
| D. | t2℃时甲、乙的饱和溶液降温到t1℃时,溶质的质量分数相等 |
10.铁、铜和银是日常生活中经常接触到的三种金属.
(1)三种金属共同具有的物理性质是导热性(或导电性、延展性等)(写出一条即可).
(2)若要证明铁、铜和银的活动性顺序,需要进行的实验有ABD(填序号).
(3)氧化铁是一种红褐色的固体粉末.请根据图1回答问题.

①写出气体X与氧化铁反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②Y溶液中的溶质为CuSO4(或CuCl2)和H2SO4(或HCl).
③写出生成无色气体E的化学方程式Fe+H2SO4═FeSO4+H2↑(或Fe+2HCl═FeCl2+H2↑).
(4)根据铁与硫酸铜溶液的反应判断,下表中x和y所表示的四种关系符合图2变化规律的是D(填序号).
(1)三种金属共同具有的物理性质是导热性(或导电性、延展性等)(写出一条即可).
(2)若要证明铁、铜和银的活动性顺序,需要进行的实验有ABD(填序号).
| A.将铁片放入盐酸中 | B.将铜片放入盐酸中 |
| C.将铁片放入硝酸银溶液中 | D.将铜片放入硝酸银溶液中 |

①写出气体X与氧化铁反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②Y溶液中的溶质为CuSO4(或CuCl2)和H2SO4(或HCl).
③写出生成无色气体E的化学方程式Fe+H2SO4═FeSO4+H2↑(或Fe+2HCl═FeCl2+H2↑).
(4)根据铁与硫酸铜溶液的反应判断,下表中x和y所表示的四种关系符合图2变化规律的是D(填序号).
| 选项 | x | y |
| A | 铁粉质量 | 溶液质量 |
| B | 铁粉质量 | 析出铜的质量 |
| C | 反应时间 | 生成硫酸亚铁的质量 |
| D | 反应时间 | 反应过程中金属质量的变化情况 |
7.下列图象分别与选项中的操作相对应,其中不合理的是( )
| A. | 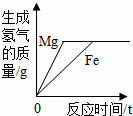 相同质量的镁粉和铁粉分别与过量且溶质质量分数相同的稀硫酸反应 | |
| B. | 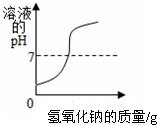 向稀盐酸中滴加过量的氢氧化钠溶液 | |
| C. |  向硝酸铜和硝酸的混合溶液中逐滴加入氢氧化钠溶液 | |
| D. | 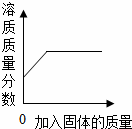 向一定量不饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化) |
4.小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想可否用
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解成氧气,可做增氧剂、杀菌剂等.
【猜想与论证】
(1)小明依据过氧化钙在300℃时可分解出氧气,提出猜想Ⅰ.
猜想Ⅰ:加热过氧化钙可制取氧气.
实验结论:加热过氧化钙可制取氧气.
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.
猜想Ⅱ:过氧化钙与水反应可制取氧气.
实验结论:不能用过氧化钙与水反应制取氧气.
分析与反思:
①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民可用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议:加热过氧化钙和水的混合物(或向过氧化钙和水的混合物中加入催化剂).
以上建议是否可行,还需进一步通过实验验证.
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解成氧气,可做增氧剂、杀菌剂等.
【猜想与论证】
(1)小明依据过氧化钙在300℃时可分解出氧气,提出猜想Ⅰ.
猜想Ⅰ:加热过氧化钙可制取氧气.
| 实验装置 | 实验主要过程 |
 | ①检验装置气密性.操作如下:想将导管伸入液面下,用手紧握试管,观察到导管口有气泡冒出,松开后,有液体进入导管. ②加入过氧化钙,加热,导管口有大量气泡冒出. ③收集一瓶气体. ④停止加热.熄灭酒精灯前,应先将导气管从移出水面. ⑤检验气体.方法是将带火星的木条放在瓶口,若木条复燃,则是氧气. |
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.
猜想Ⅱ:过氧化钙与水反应可制取氧气.
| 实验装置 | 实验主要过程 |
 | ①检验装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎看不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出. |
分析与反思:
①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民可用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议:加热过氧化钙和水的混合物(或向过氧化钙和水的混合物中加入催化剂).
以上建议是否可行,还需进一步通过实验验证.
8.下列关于分子和原子的说法正确的是( )
| A. | 分子是保持物质性质的最小粒子 | B. | 原子是化学变化中的最小粒子 | ||
| C. | 分子的质量不一定比原子的质量大 | D. | 分子是构成物质的唯一粒子 |
5.观察和实验是学习科学的重要方式,下列实验中观察到的颜色正确的是( )
| A. | 铁锈放入稀盐酸中溶液变黄色 | |
| B. | 硫酸铜溶液中滴加氢氧化钠溶液出现红褐色絮状沉淀 | |
| C. | 硫在氧气中燃烧发出微弱的淡蓝色火焰 | |
| D. | 酚酞试液滴入硫酸溶液中变红色 |