题目内容
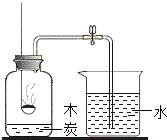
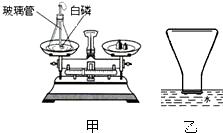
图甲是探究质量守恒的实验装置,锥形瓶内插有一根上端系有一小气球、下端能与白磷接触的玻璃管.
(1)引燃白磷,气球胀大,待锥形瓶冷却至室温后,又看到气球变瘪,其中发生反应的化学方程式为: ;在玻璃管上方系一气球的主要目的 .
(2)实验结束后(锥形瓶已冷却到室温),将锥形瓶瓶口倒置于盛满水的水槽中(如图乙所示,瓶口贴紧水面),拔下瓶塞,发现水进入锥形瓶中,则进入瓶中的水约占锥形瓶的容积的 .
(3)由质量守恒定律可知,化学反应前后,一定不变的是 .(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类
⑥物质种类.
答案 分析:(1)红磷燃烧生成五氧化二磷,反应的方程式为:4P+5O2 2P2O5;在玻璃管上方系一气球的主要目的是:防止把橡皮塞冲出;
2P2O5;在玻璃管上方系一气球的主要目的是:防止把橡皮塞冲出;
(2)白磷燃烧把空气中的氧气全部消耗掉了,而氧气约占空气体积的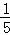 ,所以水会进入
,所以水会进入 ;
;
(3)化学反应前后原子种类、原子数目、原子的质量、元素种类、各物质的总质量都不变.因此选①②⑤.

 手拉手全优练考卷系列答案
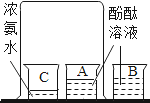
手拉手全优练考卷系列答案甲、乙、丙三位同学利用图中的装置,围绕“用称量的方法验证化学反应是否遵守质量守恒定律并分析实验条件”这一探究目的开展活动。
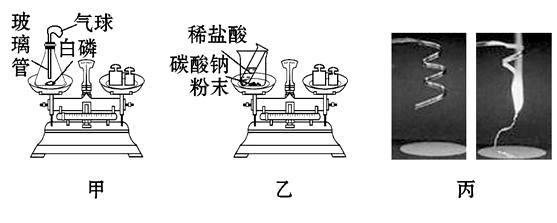
【实验步骤】①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在 两个托盘天平上,并用砝码使天平平衡。丙对石棉网和打磨干净的镁条进行称量。
两个托盘天平上,并用砝码使天平平衡。丙对石棉网和打磨干净的镁条进行称量。
②三位同学分别利用装置进行化学反应。
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡。丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量。
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析。
| 实验现象 | 实验原理 | 实验结论 | |
| 甲同学 | 4P+5O2 | 该反应遵守质量守恒定律 | |
| 乙同学 | Na2CO3+2HCl 2NaCl+H2O+CO2↑ | 该反应遵守质量守恒定律 | |
| 丙同学 | 镁条剧烈燃烧,发出耀眼白光,放热,生成白色固体,反应前后称量质量不相等 | 该反应不遵守质量守恒定律 |
(2)通过对上述实验的对比分析,甲乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的。在实验操作完 全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有 。
全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有 。
【实验结论】化学反应都遵守质量守恒定律。

 P2O5
P2O5
 反应呢?
反应呢? C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2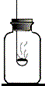 A.木炭 B.红磷 C.硫粉
A.木炭 B.红磷 C.硫粉