题目内容
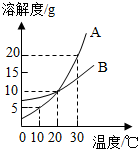 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )| A、30℃时,向100克水中加入25克A物质,充分溶解后所得溶液是饱和溶液 |
| B、20℃时A、B两物质的饱和溶液溶质质量分数相等 |
| C、A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 |
| D、30℃时,将B物质的不饱和溶液转变为饱和溶液,可以采取恒温蒸发溶剂的方法 |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据30℃时,A物质的溶解度进行分析;
B、根据溶解度曲线的含义及饱和溶液的溶质质量分数计算方法分析;
C、根据A物质的饱和溶液从30℃降温到10℃,溶解度减小,会析出晶体考虑;
D、根据不饱和溶液与饱和溶液的转化方法考虑;
B、根据溶解度曲线的含义及饱和溶液的溶质质量分数计算方法分析;
C、根据A物质的饱和溶液从30℃降温到10℃,溶解度减小,会析出晶体考虑;
D、根据不饱和溶液与饱和溶液的转化方法考虑;
解答:解:A、30℃时,A物质的溶解度是20g,是在30℃时,100g水中最多溶解20gA物质,所以30℃时,向100克水中加入25克A物质,充分溶解后所得溶液是饱和溶液,还有5g溶质没有溶解,故A说法正确;
B、20℃时A和B的溶解度相等,所以该温度的饱和溶液溶质的质量分数相等,故B正确;
C、A物质的饱和溶液从30℃降温到10℃,溶解度减小,会析出晶体,仍然是饱和溶液,故C说法错误;
D、30℃时,将B物质的不饱和溶液转变为饱和溶液,可以采取恒温蒸发溶剂、加入溶质、降低温度等方法,故D说法正确.
故选C.
B、20℃时A和B的溶解度相等,所以该温度的饱和溶液溶质的质量分数相等,故B正确;
C、A物质的饱和溶液从30℃降温到10℃,溶解度减小,会析出晶体,仍然是饱和溶液,故C说法错误;
D、30℃时,将B物质的不饱和溶液转变为饱和溶液,可以采取恒温蒸发溶剂、加入溶质、降低温度等方法,故D说法正确.
故选C.
点评:解答本题关键是要知道饱和溶液的判断,在某一温度,一定量溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液,不管是升温还是降温,只要是溶解度见小了,就会析出晶体.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质能大量共存于水溶液中的是( )
| A、NaOH和MgSO4 |
| B、AgNO3和NaCl |
| C、HNO3和KCl |
| D、Na 2CO3和CaCl2 |
下列是一些物质的自我介绍,其中介绍自己化学性质的是( )
A、 我是紫红色的固体 |
B、 我在自然界硬度最大 |
C、 我会生锈 |
D、 我在常温下是气体 |
为减缓化学反应速率,下列做法合理的是( )
| A、面团发酵时放在温热处 |
| B、在食品密封包装时充入氮气 |
| C、煤燃烧时向煤炉中鼓入空气 |
| D、用食醋除水垢时使用浓度高的食醋 |

