题目内容
1.请结合下列实验常用装置,回答有关问题.
(1)写出图中标有字母的仪器名称:a锥形瓶.
(2)若用A装置制取氧气,反应的方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若用A制取的氧气做铁丝燃烧的实验,则收集氧气的装置用D,原因是集气瓶底要预先留一些水.
(3)若要制取氢气,在B装置中装有锌粒,那么长颈漏斗中应加入稀硫酸(填写试剂名称),反应的化学方程式是Zn+H2SO4═ZnSO4+H2↑.如果用E装置收集该气体,则气体从c端进入(填“b”或“c”).
(4)实验室如用块状固体和液体无需加热制取难溶性气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是可控制发生的发生和停止.
(5)把分别盛满甲、乙、丙 三种气体的试管倒插在盛有水的烧杯中,一段时间后,观察到图2所示的现象.下列分析正确的是D(填字母代号).
A、甲、乙、丙气体都易溶于水 B、乙气体比甲气体更易溶于水
C、不可用排空气法收集甲气体 D、可以采用排水集气法收集丙气体.
分析 (1)依据常用仪器回答;
(2)A装置适用于加热固体制取气体,且试管口有棉花,是用加热高锰酸钾的方法制取氧气,铁丝燃烧实验,试管口要预先放一些水,防止燃烧生成的高温熔融物溅落炸裂瓶底,据此分析解答;
(3)实验室制取氢气用锌粒和稀硫酸混合,氢气密度比空气小;
(4)C装置可通过活塞开闭随时控制反应的发生和停止;
(5)试管内液面上升,说明气体溶于水,据此判断收集方法.
解答 解:(1)标号仪器是作为反应容器的锥形瓶;
(2)A装置适用于加热固体制取气体,且试管口有棉花,是用加热高锰酸钾的方法制取氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;铁丝燃烧实验,试管口要预先放一些水,防止燃烧生成的高温熔融物溅落炸裂瓶底,所以最好用排水法收集;
(3)实验室制取氢气用锌粒和稀硫酸混合,反应方程式是:Zn+H2SO4═ZnSO4+H2↑;氢气密度比空气小,所以应从短管进气,长管便于排尽空气;
(4)C装置中打开活塞,固液接触生成气体,关闭活塞,气体无法排出,试管内气压增大,则将液体压入长颈漏斗,固液分离,反应停止;
(5)观察图示可以看出:甲、乙试管倒插在盛有水的烧杯中,一段时间后,均有液体进入,说明这两种气体均能溶于水,而甲中进入的水比乙多,说明甲比乙更易溶于水,丙试管中无液体进入,说明不溶于水,故可用排水法收集的是丙气体;不知甲能否与空气中成分反应,无法判断是否能用排空气法收集;
故答案为:(1)锥形瓶;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;D;
(3)稀硫酸;Zn+H2SO4═ZnSO4+H2↑;c;
(4)D.
点评 本题主要考查常用气体的反应原理、装置的选取方法等知识;正确书写化学方程式,并会应用所学知识分析解答相关问题才能正确解答.

 根据如图提供的信息进行判断,下列说法中错误的是( )
根据如图提供的信息进行判断,下列说法中错误的是( )| A. | 该粒子属于金属元素 | B. | 该粒子易形成阴离子 | ||
| C. | 该粒子原子核内有11个质子 | D. | 该粒子呈电中性 |
| A. | H2SO4 | B. | CuSO4 | C. | ZnSO4 | D. | AgNO3 |
| A. | 2Cl | B. | 2Cl2 | C. | SO2 | D. | 2NO2 |
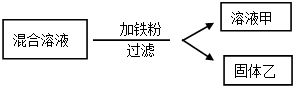 向Cu(NO3)2、AgNO3、Mg(NO3)2的混合溶液加入一定量的铁粉,充分反应后过滤.
向Cu(NO3)2、AgNO3、Mg(NO3)2的混合溶液加入一定量的铁粉,充分反应后过滤.