题目内容
7.蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收.丙氨酸(化学式为C3H7O2N)就是其中的一种.请回答下列问题;(1)丙氨酸由4种元素组成的,其相对分子质量为89;丙氨酸中碳和氢元素的原子个数比为3:7.
(2)丙氨酸中氮元素的质量分数为15.7%(计算结果精确到0.1%)
分析 (1)根据丙氨酸的化学式可知其元素组成、相对分子质量、丙氨酸分子中C、H原子个数比进行解答;
(2)丙氨酸中氮元素的质量分数为:$\frac{氮的相对原子质量×氮原子个数}{丙氨酸的相对分子质量}×100%$.
解答 解:(1)根据丙氨酸的化学式可知丙氨酸由碳、氢、氧、氮四种元素组成;它的相对分子质量=12×3+1×7+16×2+14=89;丙氨酸分子中C、H原子个数比=3:7;
故填:4;89;3:7;
(2)丙氨酸中氮元素的质量分数为:$\frac{14}{89}×100%$≈15.7%;故填:15.7%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
17.小明对铁的锈蚀进行如下探究.室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如表.
(1)实验①和②说明NaCl可以加快 (填“加快”或“减慢”)铁锈蚀的速率.
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是放热 (填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是Fe2O3•xH2O[Fe2O3或Fe(OH)3];.
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是20.5%(保留3位有效数字).
(6)现仅提供:置筒、大烧杯、玻璃棒、水、滤纸包(内含1g铁粉、O.2g碳、10滴水和少量NaCl),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,在图中画出实验装置示意图即可(注明滤纸包的位置).

| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1 g铁粉、0.2 g碳和10滴水 | 100 | 70 | 约120 |
| ② | l g铁粉、0.2 g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
| ③ | | 0 | 0 | 0 |
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是放热 (填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是Fe2O3•xH2O[Fe2O3或Fe(OH)3];.
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是20.5%(保留3位有效数字).
(6)现仅提供:置筒、大烧杯、玻璃棒、水、滤纸包(内含1g铁粉、O.2g碳、10滴水和少量NaCl),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,在图中画出实验装置示意图即可(注明滤纸包的位置).

18.某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成.分四次取样品与稀硫酸反应,其实验数据记录如表.
试计算:
(1)在四份样品所做的实验中,硫酸有剩余的是3、4;
(2)列式计算所用稀硫酸中溶质的质量分数
(3)请在图中画出在50.0g样品中加入稀硫酸的质量与产生气体质量变化关系的示意图.
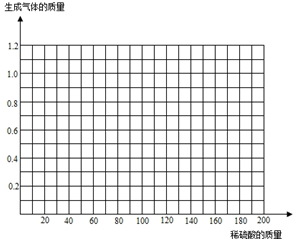
(4)请计算恰好完全反应时溶液中溶质的质量分数.
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量 | 0.4 | 0.8 | 1.0 | 1.0 |
(1)在四份样品所做的实验中,硫酸有剩余的是3、4;
(2)列式计算所用稀硫酸中溶质的质量分数
(3)请在图中画出在50.0g样品中加入稀硫酸的质量与产生气体质量变化关系的示意图.

(4)请计算恰好完全反应时溶液中溶质的质量分数.
2.对有关实验现象描述正确的是( )
| A. | 红磷在空气中燃烧发出明亮的蓝紫色火焰,同时有大量的白烟生成 | |
| B. | 木炭在空气中加热,出现红热现象 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| D. | 硫在氧气中燃烧发出淡蓝色火焰 |
12.现有化学反应A+B═C,将x克A和y克B在适当的条件下充分反后,分析得剩余物为混合物,则生成C物质的质量为( )
| A. | 等于(x+y)克 | B. | 小于(x+y)克 | C. | 大于(x+y)克 | D. | 不大于(x+y)克 |
19.下列有关催化剂的说法中错误的是( )
| A. | 催化剂就是二氧化锰 | |
| B. | 催化剂能改变其他物质的化学反应速度 | |
| C. | 在化学反应前后催化剂的质量没有改变 | |
| D. | 在化学反应前后催化剂的化学性质没有改变 |
16.下列关于氧气性质的叙述正确的是( )
| A. | 氧气易溶于水 | |
| B. | 氧气具有可燃性,是一种氧化剂 | |
| C. | 氧气的密度比空气略大 | |
| D. | 化学性质活泼,常温下能跟所有物质发生反应 |
17.分类、类比是学习化学常用的方法.
(1)初中化学有许多实验,为了便于研究我们可以把化学实验从“实验装置、物质的性质、探究的方法”等角度进行分类.据此应将下列实验中的D与①C(填“A”或“B”或“C”)归为一类,依据是②探究物质的性质.
(2)许多物质的命名与元素的化合价高低有关,如氯化铁、氯化亚铁,其中铁元素的化合价分别为+3、+2.汞元素的化合价有+2、+1两种,由此推测氧元素和+1价汞元素组成的化合物的名称为①氧化亚汞,化学式为②Hg2O.
(1)初中化学有许多实验,为了便于研究我们可以把化学实验从“实验装置、物质的性质、探究的方法”等角度进行分类.据此应将下列实验中的D与①C(填“A”或“B”或“C”)归为一类,依据是②探究物质的性质.
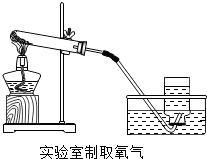 | 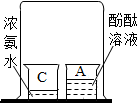 | 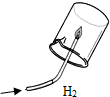 |  |
| A | B | C | D |