题目内容
8.某同学配制50g溶质质量分数为5%的KCl溶液,准备了下列实验用品.请回答下列问题:
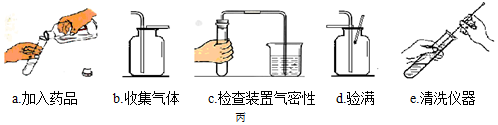
(1)该同学按下列实验步骤进行:①计算、②称量、③量取、④溶解(填步骤名称)⑤装瓶,贴标签.
(2)实验过程中除缺少细口瓶还缺少的一种玻璃仪器是玻璃棒.
(3)为了达到本实验目的,应用50(填“10”、“50”或“100”)mL量筒量取本实验所需的水倒入烧杯中.在量取水的体积时,小红同学俯视读数,则所配制溶液中氯化钾的质量分数偏大(填“偏大”、“偏小”或“不变”).
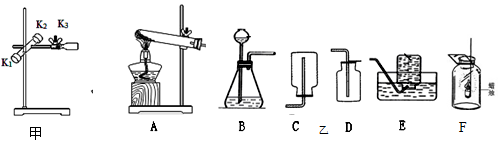
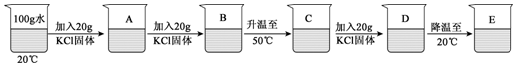
(4)已知20℃时氯化钾的溶解度是34.0g,50℃时氯化钾的溶解度是42.6g,通过如图所示的实验操作得到相应的溶液,在所得溶液中,溶质的质量分数相同的是BE(填序号).
分析 (1)该同学按下列实验步骤进行:①计算、②称量、③量取、④溶解、⑤装瓶,贴标签;
(2)实验过程中除缺少细口瓶还缺少的一种玻璃仪器是玻璃棒;
(3)选择量筒时,量程应该大于或等于量取的液体体积;
在量取水的体积时,俯视读数会导致量取液体体积偏小,从而导致所配制溶液中氯化钾的质量分数偏大;
(4)饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%.
解答 解:(1)该同学按下列实验步骤进行:①计算、②称量、③量取、④溶解、⑤装瓶,贴标签.
(2)实验过程中除缺少细口瓶还缺少的一种玻璃仪器是玻璃棒.
(3)需要水的体积为:(50g-50g×5%)÷1g/mL=47.5mL,因此应用50mL量筒量取本实验所需的水倒入烧杯中;
在量取水的体积时,小红同学俯视读数,会导致量取液体体积偏小,从而导致所配制溶液中氯化钾的质量分数偏大.
(4)A是20℃时氯化钾的不饱和溶液,B是20℃时氯化钾的饱和溶液,因此B的质量分数大于A的质量分数;
升温至50℃时C是氯化钾的不饱和溶液,质量分数大于B,再加入20g氯化钾后变成氯化钾的饱和溶液,D的质量分数大于C的质量分数,降温至20℃时,E是氯化钾的饱和溶液,因此E的质量分数和B的质量分数相等,在所得溶液中,溶质的质量分数相同的是BE.
故填:溶解;玻璃棒;50;偏大;BE.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
17.用分子的观点解释下列事实,其中不正确的是( )
| A. | 水沸腾后壶盖被顶起--温度升高,分子体积变大 | |
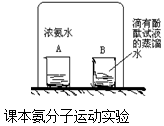
| B. | 春天百花盛开,花香四溢--分子在不断运动 | |
| C. | 50mL水和50mL酒精混合后,液体总体积小于100mL--分子之间有间隔 | |
| D. | 氧化汞受热分解--分子在化学变化中可以再分 |