题目内容
9. 全世界每年因生锈损失的钢铁,约占世界年产量的十分之一.
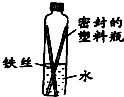
全世界每年因生锈损失的钢铁,约占世界年产量的十分之一.(1)图为某化学兴趣小组同学设计的观察铁制品锈蚀的实验装置.请你分析,以下相关叙述中正确的是B、D
A.此实验设计必须在玻璃仪器中进行
B.一段时间后,塑料瓶会变瘪,说明铁生锈与空气有关
C.一段时间后,铁丝会由下到上出现锈蚀现象
D.一段时间后,水面处铁丝锈蚀最严重
(2)为预防金属制品锈蚀,有同学提出下列措施.你认为不当的是C
A.将使用后的菜刀洗净擦干 B.在铁制门窗表面喷涂油漆
C.用钢丝刷擦去铝锅表面的氧化膜 D.在铁制水管表面镀一层锌.
分析 本题通过实验考查铁生锈的条件,铁生锈是铁与氧气与水发生的一系列复杂的化学反应.防止金属生锈的方法就是要使就是与水和氧气隔绝.
解答 解:(1)铁在潮湿空气中与氧气、水共同作用而生锈.
A、做铁制品锈蚀条件实验可以用试管也可以用题给装置进行,只要能观察到明显的实验现象即可,与采用何种仪器无关,故选项错误.
B、因铁生锈会消耗空气中的氧气,导致塑料瓶内压强减小,在大气压作用下,塑料瓶变瘪,说明空气与铁生锈有关,故选项正确.
C、铁制品与水面接触部位生锈最严重,因这部分与空气和水都充分接触了.所以水面处铁丝锈蚀严重,故选项错误.
D、由C选项分析可知,D选项正确.
故选B、D.
(2)A、使用后的菜刀洗净擦干有利于防锈,故正确;
B、在铁制门窗表面喷涂油漆,使铁与水和氧气隔绝,有利于防锈,故正确;
C、铝锅表面的氧化膜对铝锅起到保护作用,阻止铝被进一步氧化,故擦去是错误的.
D、在铁制水管表面镀一层锌,使铁与水和氧气隔绝,有利于防锈,故正确;
故选C.
点评 解答本题要掌握金属生锈的条件,只有这样才能找出防止金属生锈的方法.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
20.极细铁粉可做抗氧剂和干燥剂.现有一包从食品袋中取出的这样的干燥剂,对它成分进行探究并完成下表.
(1)提出问题:这包干燥剂的成分是什么?①铁②氧化铁③氧化铁和铁的混合物.
(2)实验探究:
最终结论是这包粉末是铁和氧化铁的混合物.
(1)提出问题:这包干燥剂的成分是什么?①铁②氧化铁③氧化铁和铁的混合物.
(2)实验探究:
| 操作 | 现象 | 结论 |
| 用磁铁吸引 | 黑色粉末被吸附,剩余红色粉末 | 粉末是铁和氧化铁的混合物 |
| 加入稀盐酸 | 粉末减少,有气体生成,溶液有无色逐渐变成黄绿色 | 粉末是铁和氧化铁的混合物 |
4.下列事实与对应的解释相符合的是( )
| A. | 空气能被压缩 分子体积可以变小 | |
| B. | 甘蔗甜,苦瓜苦 不同分子性质不同 | |
| C. | 结冰的水不能流动 0℃以下,水分子不再运动 | |
| D. | 50mL水和50mL酒精混合后的总体积小于100mL 分子的质量和体积都很小 |
14.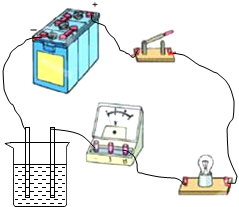 电解质是溶于水或熔化状态下能导电的化合物.为了研究电解质溶液的导电能力
电解质是溶于水或熔化状态下能导电的化合物.为了研究电解质溶液的导电能力
与什么因素有关,某同学设计了如图的一个实验方案,并实验得到了如上表的数据:(已知纯水不导电)
(1)你从实验数据得出的结论是电解质溶液的导电性与溶质的种类、质量分数有关(只要写出一个即可).
(2)假如烧杯中盛有200克的氢氧化钡溶液,要使电流表的示数等于0.09A,则此氢氧化钡溶液中含有氢氧化钡的质量为6克;用胶头滴管不断往氢氧化钡溶液中滴加硫酸溶液,实验中可以观察到的现象有溶液变浑浊,电流表的电流先减小趋于零而后增大,小灯泡由亮变暗、熄灭,而后又变亮.
(3)若图中灯泡的额定电压为12伏,额定功率为3瓦,当烧杯中的溶液是4%的Ca(NO3)2溶液时,灯泡的实际功率是1.6W.(保留1位小数)
 电解质是溶于水或熔化状态下能导电的化合物.为了研究电解质溶液的导电能力
电解质是溶于水或熔化状态下能导电的化合物.为了研究电解质溶液的导电能力与什么因素有关,某同学设计了如图的一个实验方案,并实验得到了如上表的数据:(已知纯水不导电)
| 溶质质量分数 电流强度 溶液 | 2% | 3% | 4% |
| Ca(NO3)2溶液 | 0.09A | 0.14A | 0.18A |
| Ba(OH)2溶液 | 0.06A | 0.09A | 0.11A |
(2)假如烧杯中盛有200克的氢氧化钡溶液,要使电流表的示数等于0.09A,则此氢氧化钡溶液中含有氢氧化钡的质量为6克;用胶头滴管不断往氢氧化钡溶液中滴加硫酸溶液,实验中可以观察到的现象有溶液变浑浊,电流表的电流先减小趋于零而后增大,小灯泡由亮变暗、熄灭,而后又变亮.
(3)若图中灯泡的额定电压为12伏,额定功率为3瓦,当烧杯中的溶液是4%的Ca(NO3)2溶液时,灯泡的实际功率是1.6W.(保留1位小数)
1.关于“舌尖上的化学”,下列说法不科学的是( )
| A. | 为了身体健康,必须均衡膳食 | |
| B. | 为预防缺碘性疾病,可食用适量海带 | |
| C. | 为使发面食品松软可口,制作时可添加适量碳酸氢钠 | |
| D. | 为延长食品保质期,在食品中添加大量防腐剂 |
18.某同学在自主学习酸的知识时,设计了以下实验报告,请将其补充完整.
【实验目的】探究(或认识)稀酸的通性.
【实验用品】试管、铁片、铜片、稀盐酸、稀硫酸、NaOH溶液、石蕊和酚酞溶液等.
【实验内容】
【实验思考】从物质组成的角度解释酸具有通性的原因酸都含有氢元素.
【实验目的】探究(或认识)稀酸的通性.
【实验用品】试管、铁片、铜片、稀盐酸、稀硫酸、NaOH溶液、石蕊和酚酞溶液等.
【实验内容】
| 实验 步骤 |  | 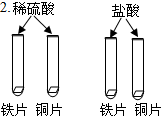 | 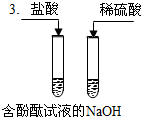 |
| 实验 现象 | 溶液变为 红色 | 稀酸中的铁片表面都有 气泡产生,铜片表面都没有明显现象 | 溶液由红色变为 无色 |
| 分析 与 结论 | 结论:稀酸能与指示剂作用 | 铁与稀硫酸反应的化学方程式为Fe+H2SO4═FeSO4+H2↑ 结论:稀酸能与活泼金属反应 | 结论: 酸能和碱反应 |
3.下列实验操作正确的是( )
| A. | 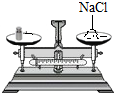 称取食盐 | B. | 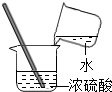 稀释浓硫酸 | C. | 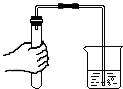 检查气密性 | D. | 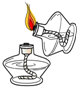 点燃酒精灯 |