题目内容
20.某同学在参考书上发现,镁能在二氧化碳气体中燃烧,于是他到实验室里做了如下实验:将镁条用砂纸擦亮,点燃后迅速伸人盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,产生一种白色粉末和一种黑色粉末.你认为他的结论不正确的是( )| A. | 金属镁着火不能用二氧化碳灭火 | |
| B. | 该反应放出热量 | |
| C. | 该反应的实质是Mg夺取了CO2中的氧,CO2发生了还原反应 | |
| D. | 该反应是分解反应 |
分析 本题由同学自行实验中的发现,给出了一个的新信息,要求通过所给实验的阅读分析,对相关结论进行评价.解题时,要抓住关键词:①镁条剧烈燃烧,发出白光,②产生一种白色粉末(MgO)和一种黑色粉末(C),由此推出答案.
解答 解:A、一般情况下,二氧化碳不能燃烧,也不能支持燃烧.由题中的信息:“发现镁条剧烈燃烧,发出白光”,说明镁能在C02中燃烧,所以镁条燃烧时不能用二氧化碳来灭火,故A正确;
B、镁和二氧化碳反应生成氧化镁和碳现象为剧烈燃烧,故要放出热量,故B正确;
C、镁和二氧化碳反应生成氧化镁和碳,其化学方程式为:2Mg+C02$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,所以镁是得到氧的物质,具有还原性,二氧化碳发生了还原反应,故C正确;
D、镁和二氧化碳反应生成氧化镁和碳,其化学方程式为:2Mg+C02$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,所以不是一种物质生成两种或两种以上物质的分解反应,故D不正确.
故选:D.
点评 二氧化碳是化学中需要掌握的一种重要物质,二氧化碳内容的考查也是历年各地学业评价考试的热点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列变化中,与其它变化有根本区别的一种是( )
| A. | 水结成冰 | B. | 木材加工成课桌 | C. | 食物腐败 | D. | 石蜡融化 |
11.做化学实验时,我们要关注物质的变化,下列物质在氧气中燃烧,火星四射,生成黑色固体的是( )
| A. | 铁丝 | B. | 镁条 | C. | 木炭 | D. | 红磷 |
8.对“20%的白砂糖水溶液”含义解释错误的是( )
| A. | 40g水中溶解了10g白砂糖 | |
| B. | 将白砂糖与水按照1:9的质量比配成的溶液 | |
| C. | 将20g白砂糖溶于80g水中所得的溶液 | |
| D. | 100g白砂糖溶液中溶解了20g白砂糖 |
15.如图是金刚石,石墨,C60,碳纳米管的结构示意图,下列说法正确的是( )
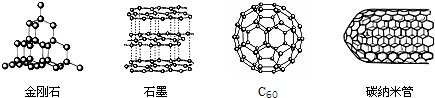

| A. | 四种物质都是只由碳元素组成,故是同一种碳单质 | |
| B. | 四种物质中碳纳米管是一种新型化合物 | |
| C. | 四种物质完全燃烧后的产物都是CO2 | |
| D. | 四种物质中金刚石与石墨的碳原子的结构不同 |
5.加油站必须张贴的安全标志是( )
| A. |  | B. |  | C. |  | D. |  |
10.下列化学方程式符合变化事实的是( )
| A. | 用电解水的方法测定水的组成:2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ | |
| B. | 用稀盐酸除去铁锈的反应:Fe2O3+6HCl═2FeCl3+3H2↑ | |
| C. | 赤铁矿炼铁:3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2 | |
| D. | 用二氧化碳制碳酸饮料:CO2+H2O═H2CO3 |
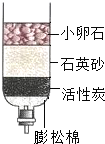 结合某地在抗旱过程中的一些做法,回答问题:
结合某地在抗旱过程中的一些做法,回答问题: