题目内容
12.人类生活离不开金属.(1)某“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.铁生锈是铁与水、氧气等物质共同作用的结果.
(2)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议回收再利用废旧金属.(答一点即可)
(3)铝比铁有更好的抗腐蚀性能,原因是铝的表面能生成一层氧化铝保护膜;
(4)铜可以拉成铜丝,这是利用了金属的延展性;
(5)“沙里淘金”说明金在自然界中以单质(填“单质”或“化合物”)形式存在;
(6)金属锰单质化学性质较活泼,易与稀硫酸反应生成+2价锰的化合物和一种气体单质,试写出相关化学方程式Mn+H2SO4=MnSO4+H2↑.
分析 (1)从铁生锈的条件考虑,铁只有与水、空气同时接触时才生锈来分析;
(2)回收再利用废旧金属资源是保护金属资源的一种重要方法;
(3)根据铝会与空气中的氧气反应生成致密的氧化铝薄膜进行分析;
(4)根据铜可以制成铜丝是利用了铜的延展性进行分析;
(5)根据金的化学性质非常稳定,在自然界中主要是以单质形式存在进行解答;
(6)根据反应的原理来分析解答.
解答 解:(1)铁与水单独接触,或单独与氧气接触,都不容易生锈,只有与水和氧气同时接触时才容易生锈;发热剂需要接触到空气才会发热,原因是铁要与水、氧气等共同作用才会生锈.故填:水、氧气.
(2)为了保护金属资源,除防止金属的腐蚀外,回收再利用废旧金属也是保护金属资源的一种重要方法.故填:回收再利用废旧金属;
(3)铝制品比铁制品有更好的抗腐蚀性能,原因是铝的表面能生成一层致密的氧化膜阻止铝的进一步氧化;故填:氧化铝保护膜;
(4)铜可以制成铜丝是利用了铜的延展性;故填:延展;
(5)元素的存在形式由其化学性质决定,沙里淘金,说明金的化学性质稳定,与土壤中的水及氧气等物质不反应,在自然界主要以单质的形式存在.故答案为:单质.
(6)锰与稀硫酸反应生成硫酸锰和氢气;故填:Mn+H2SO4=MnSO4+H2↑.
点评 本题考查了的知识点较多,但属于基本化学知识的考查,难度不大.

练习册系列答案
相关题目
7.下列实验操作错误的是( )
| A. | 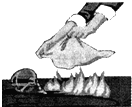 酒精灯失火用湿布铺盖 | B. | 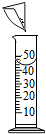 将NaCl倒入量筒中配制溶液 | ||
| C. |  加碱研磨后闻气味鉴别铵态氮肥 | D. | 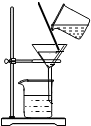 分离溶液中析出的KNO3 |
17.下列各组物质中,带点的同种元素的化合价相同的是( )
| A. | Cl2、NaCl | B. | NH4Cl、HNO3 | C. | MnO2、K2MnO4 | D. | SO2、H2SO3 |
1.下列应用,对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 用X射线检查胃肠时,让病人服用钡餐:BaCO3+2HCl═BaCl2+H2O+CO2↑复分解反应 | |
| B. | 美丽的溶洞中钟乳石的形成:Ca(HCO3)2═CaCO3↓+CO2↑+H2O 分解反应 | |
| C. | 用木炭测空气中氧气含量:C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2 化合反应 | |
| D. | 用铁桶盛装稀硫酸:Fe+H2SO4═FeSO4+H2↑ 置换反应 |