题目内容
5.在登山过程中,人均携带16kg的氧气.若实验室用高锰酸钾为原料,制取同质量的氧气,需多少千克的高锰酸钾?分析 高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,由生成氧气的质量,由反应的化学方程式列式计算出需要高锰酸钾的质量即可.
解答 解:设需要高锰酸钾的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 16kg
$\frac{316}{32}=\frac{x}{16kg}$ x=158kg
答:需158千克的高锰酸钾.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
15.将6g两种金属的混合物粉末投入一定量的稀盐酸中,产生0.2g氢气.则下列各组金属中肯定不能构成上述混合物的是( )
| A. | Fe、Cu | B. | Mg、Fe | C. | Ag、Mg | D. | Zn、Mg |
16.学习化学的一个重要途径是科学实验探究,下列化学实验操作不正确的是( )
| A. |  液体的倾倒 | B. |  液体的量取 | C. |  点燃酒精灯 | D. | 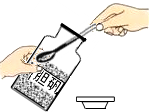 取固体药品 |
13.下列现象的微观解释中,不正确的是( )
| A. | 氢气和液氢都可做燃料--相同物质的分子,其化学性质相同 | |
| B. | 桂花盛开花香四溢--分子在不断运动 | |
| C. | 用水银温度计测量体温--温度升高,原子间空隙变大 | |
| D. | 水烧开后易把壶盖冲起--温度升高,分子变大 |
8.有一无色液体X,分成等量的三份,向其中分别加入少量的H2SO4溶液、Ba(OH)2溶液、KCl溶液,产生的现象如表.则该无色液体X是下列各项中的( )
| 加入物质 | H2SO4溶液 | Ba(OH)2溶液 | KCl溶液 |
| 现象 | 有气泡产生 | 产生白色沉淀 | 无明显现象 |
| A. | NaCl溶液 | B. | 稀盐酸 | C. | 酚酞试液 | D. | Na2CO3溶液 |
6.下列仪器中,不属于玻璃仪器的是( )
| A. | 烧杯 | B. | 集气瓶 | C. | 试管夹 | D. | 酒精灯 |
 铕是一种稀土元素,如图是元素周期表中铕元素的相关信息,下列说法正确的是B
铕是一种稀土元素,如图是元素周期表中铕元素的相关信息,下列说法正确的是B