题目内容
某K2CO3样品,可能含有Na2CO3、MgCO3、NaCl中的几种杂质.取该样品6.9g,加入50g稀盐酸中,恰好完全反应得到无色溶液,同时产生2.2g气体.下列判断正确的是( )
| A、样品中一定没有MgCO3 |
| B、NaCl不与盐酸反应,说明样品中一定没有NaCl |
| C、所加稀盐酸中溶质的质量分数为7.3% |
| D、Na2CO3和MgCO3都能和稀盐酸反应生成气体,说明样品中一定有Na2CO3和MgCO3 |
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:推断混合物的可能组成
分析:根据生成的二氧化碳求得盐酸的质量分数和所需碳酸钾的质量,然后推测其他的成分.
解答:解:设生成2.2g二氧化碳需要碳酸钾的质量为x,纯盐酸的质量为y,则有
K2CO3+2HCl=2KCl+CO2↑+H2O
138 73 44
x y 2.2g
=
x=6.9g
=
y=3.65g
根据计算可以知道即使全部是碳酸钾也只能生成2.2g二氧化碳,但是题干中给的信息是:K2CO3固体样品不纯,所以根据近似平均值法,则其中混有的杂质:一种产生二氧化碳的能力比碳酸钾强,另一种产生二氧化碳的能力比碳酸钾弱;根据质量守恒定律可以知道,碳酸根中的碳元素和二氧化碳中的碳元素的质量相等,可以通过比较碳酸根的含量,来确定生成二氧化碳气体质量的多少,在碳酸钾中,含碳酸根为
×100%=43.5%,在碳酸钠中,含碳酸根为
×100%=56.6%,在碳酸镁中,含碳酸根为
×100%=71.4%,碳酸钠和碳酸镁中碳酸根的含量都比碳酸钾中碳酸根的含量高,即在质量相同的条件下碳酸根含量多的物质,生成二氧化碳气体的质量也要大,所以可以判断一定含有氯化钠,但是对于碳酸钠和碳酸镁这两种物质中可能含有一种,也可能是两种都存在,故选项A、B、D的判断是错误的;
所加稀盐酸中溶质的质量分数是:
×100%=7.3%,C正确;
故选C.
K2CO3+2HCl=2KCl+CO2↑+H2O
138 73 44
x y 2.2g
| 138 |
| x |
| 44 |
| 2.2g |
x=6.9g
| 73 |
| y |
| 44 |
| 2.2g |
y=3.65g
根据计算可以知道即使全部是碳酸钾也只能生成2.2g二氧化碳,但是题干中给的信息是:K2CO3固体样品不纯,所以根据近似平均值法,则其中混有的杂质:一种产生二氧化碳的能力比碳酸钾强,另一种产生二氧化碳的能力比碳酸钾弱;根据质量守恒定律可以知道,碳酸根中的碳元素和二氧化碳中的碳元素的质量相等,可以通过比较碳酸根的含量,来确定生成二氧化碳气体质量的多少,在碳酸钾中,含碳酸根为
| 60 |
| 138 |
| 60 |
| 106 |
| 60 |
| 84 |
所加稀盐酸中溶质的质量分数是:
| 3.65g |
| 50g |
故选C.
点评:熟练掌握碳酸盐的性质,学会利用近似平均值的方法结合质量守恒定律定律来解答这类题目:先假设全部是主要的物质,然后根据计算的数据,判断是否含有其他的物质,这是解答此题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有一首儿歌这样唱到:“大自然真奇妙,看不见摸不着,有鼻子少不了,是天下宝中宝.”描述的是人的呼吸离不了空气,这是因为空气中有( )
| A、氮气 | B、氧气 |
| C、二氧化碳 | D、稀有气体 |
下列各组离子在水溶液里能大量共存是( )
| A、Fe2+、K+、Cl-、Ag+ |
| B、Ba2+、Na+、CO32-、SO42- |
| C、NH4+、Na+、OH-、NO3- |
| D、Na+、K+、CO32-、Cl- |
下列符号与对应结构示意图的描述中,不正确的是( )
A、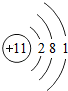 Na Na |
B、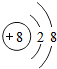 O2+ O2+ |
C、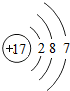 Cl Cl |
D、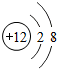 Mg2+ Mg2+ |
 在高楼林立的哈尔滨,有一座28层的建筑,该建筑是采用新技术建造的.与传统建筑方式相比,可节省15.7%的用钢量、l5.8%的混凝土量、53.4%的模板量和12%的人工量,单体工程主体结构能够减少碳排放8.3%.下列有关叙述中不正确的是( )
在高楼林立的哈尔滨,有一座28层的建筑,该建筑是采用新技术建造的.与传统建筑方式相比,可节省15.7%的用钢量、l5.8%的混凝土量、53.4%的模板量和12%的人工量,单体工程主体结构能够减少碳排放8.3%.下列有关叙述中不正确的是( )| A、钢和生铁,都属于金属材料 |
| B、钢筋混凝土属于复合材料 |
| C、楼内装修时,粉刷墙壁所用石灰浆的主要成分为碳酸钙 |
| D、减少碳排放对保护环境有重要意义,值得提倡 |
蜡烛(足量)在如图1所示的密闭容器内燃烧至熄灭,用仪器测出这一过程中瓶内氧气含量的变化(如图2所示).下列判断中,不正确的是( )
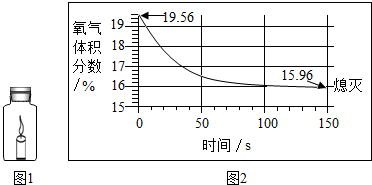

| A、瓶中氧气浓度小于一定值时,蜡烛无法燃烧 |
| B、实验过程中瓶中二氧化碳的含量增大 |
| C、该过程中瓶内物质总质量不变 |
| D、蜡烛熄灭原因是瓶内没有了氧气 |