题目内容
一氧化碳和氧气的混合气体48g,在密闭容器中点燃后,充分反应,得到二氧化碳44g,则原混合气体中一氧化碳的质量为
- A.16g
- B.20g
- C.28g
- D.32g
CD
分析:根据质量守恒定律可知一氧化碳和氧气的混合气体48g,充分反应,得到二氧化碳44g说明有气体剩余,剩余气体质量为48g-44g=4g,剩余气体可能是一氧化碳,也可能是氧气,再根据方程式计算出参加反应的一氧化碳的质量再进行讨论即可.
解答:根据质量守恒定律可知剩余气体质量为48g-44g=4g,剩余气体可能是一氧化碳,也可能是氧气,设生成44g二氧化碳需要参加反应的一氧化碳质量为x则:
2CO+O2 2CO2
2CO2
56 88
x 44g
根据: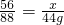 解得x=26g,所以一氧化碳质量可能是28g,也可能是28g+4g=32g.
解得x=26g,所以一氧化碳质量可能是28g,也可能是28g+4g=32g.
故选CD.
点评:解答本题关键是要根据质量守恒定律分析出反应物过量,再根据生成物质量计算出实际参加反应的反应物质量,再根据反应物过量情况进行分析.
分析:根据质量守恒定律可知一氧化碳和氧气的混合气体48g,充分反应,得到二氧化碳44g说明有气体剩余,剩余气体质量为48g-44g=4g,剩余气体可能是一氧化碳,也可能是氧气,再根据方程式计算出参加反应的一氧化碳的质量再进行讨论即可.
解答:根据质量守恒定律可知剩余气体质量为48g-44g=4g,剩余气体可能是一氧化碳,也可能是氧气,设生成44g二氧化碳需要参加反应的一氧化碳质量为x则:
2CO+O2
 2CO2
2CO256 88
x 44g
根据:
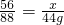 解得x=26g,所以一氧化碳质量可能是28g,也可能是28g+4g=32g.
解得x=26g,所以一氧化碳质量可能是28g,也可能是28g+4g=32g.故选CD.
点评:解答本题关键是要根据质量守恒定律分析出反应物过量,再根据生成物质量计算出实际参加反应的反应物质量,再根据反应物过量情况进行分析.

练习册系列答案
相关题目

