题目内容
为什么酒越陈越香?原来白酒的主要成分是乙醇,把酒埋在地下,保存好,放置几年后,乙醇就和白酒中较少的成分乙酸发生化学反应,生成的C4H8O2(乙酸乙酯)具有果香味.上述反应速度较慢,但时间越长,也就有越多的乙酸乙酯生成,因此酒越陈越香.下列有关乙酸乙酯的说法正确的是( )
| A、乙酸乙酯由3种元素组成 |
| B、一个乙酸乙酯分子中含有一个氧分子 |
| C、乙酸乙酯由14个原子构成 |
| D、乙酸乙酯中碳元素与氧元素的质量比为2:1 |
考点:化学式的书写及意义,元素质量比的计算
专题:化学用语和质量守恒定律
分析:A、根据乙酸乙酯的化学式进行分析其元素组成;
B、根据分子是由原子构成的进行判断;
C、根据乙酸乙酯的化学式的意义进行分析;
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答.
B、根据分子是由原子构成的进行判断;
C、根据乙酸乙酯的化学式的意义进行分析;
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答.
解答:解:A、根据乙酸乙酯的化学式可知,乙酸乙酯由C、H、O三种元素组成;故A说法正确;
B、分子是由原子构成的,一个乙酸乙酯分子中含有2个氧原子,不含氧分子;故B说法错误;
C、一个乙酸乙酯分子由14个原子构成;故C说法错误;
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得乙酸乙酯中碳、氧元素质量比为(12×4):(16×2)=3:2;故D说法错误.
故选:A.
B、分子是由原子构成的,一个乙酸乙酯分子中含有2个氧原子,不含氧分子;故B说法错误;
C、一个乙酸乙酯分子由14个原子构成;故C说法错误;
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得乙酸乙酯中碳、氧元素质量比为(12×4):(16×2)=3:2;故D说法错误.
故选:A.
点评:本题考查学生根据化学式确定组成物质元素及原子个数、元素质量比计算方法的掌握,进行解题的能力.

练习册系列答案
相关题目
下列溶液中分别放入锌粒,一段时间后取出,溶液质量减少的是( )
| A、MgCl2 溶液 |
| B、稀盐酸 |
| C、硫酸亚铁溶液 |
| D、AgNO3溶液 |
已知同温、同压下,相同体积的任何气体,都含有相同数目的分子.在一个密闭容器中盛有H2、O2、Cl2组成的混合气体.通过电火花引爆后,三种气体恰好完全反应.经充分冷却后,所得溶液中溶质的质量分数为33.4%,则原混合气体中H2、O2、Cl2分子数目简单整数比是(( )
| A、1:1:1 |
| B、3:2:1 |
| C、1:2:3 |
| D、9:4:1 |
为探究Fe、Cu、Ag 三种金属的活动性顺序,某兴趣小组设计了如图所示的四组实验方案,你认为不可行的是( )
A、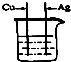 FeSO4溶液 |
B、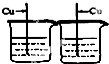 FeSO4溶液 AgNO3溶液 |
C、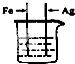 CuSO4溶液 |
D、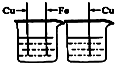 稀盐酸 AgNO3溶液 |
下列化学方程式书写正确的是( )
A、4Fe+3O2
| ||||
B、2H2+O2
| ||||
| C、Zn+H2SO4═ZnSO4+H2↑ | ||||
D、4P+5O2
|
稀有气体的用途越来越广,以下用途利用了稀有气体化学性质的是( )
| A、利用氦气填充气球 |
| B、利用稀有气体作保护气 |
| C、利用稀有气体制霓虹灯 |
| D、利用稀有气体制照明光源 |
6月5日是世界环境日,“低碳减排,绿色生活”,下列说法或做法不符合低碳理念的是( )
| A、日常生活提倡用布袋代替塑料袋 |
| B、公交出行,少用私车 |
| C、为便于使用,电脑一直处于待机状态 |
| D、随手关灯,节约用电 |
下列反应属于分解反应的是( )
| A、蜡烛在空气中燃烧 |
| B、硫在氧气中燃烧 |
| C、加热高锰酸钾 |
| D、分离液态空气 |