题目内容
A、B、C、D是四种粒子的结构示意图,请你回答:
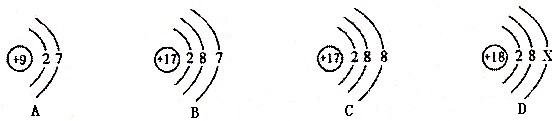
(1)D图中X=
(2)图中属于同种元素的是
(3)图中粒子化学性质相似的是
(4)B粒子与Mg2+形成的化合物的化学式是

(1)D图中X=
8
8
;(2)图中属于同种元素的是
BC
BC
(填序号),理由是具有相同的质子数(或核电荷数)
具有相同的质子数(或核电荷数)
;(3)图中粒子化学性质相似的是
A和B
A和B
(填序号),它们在化学反应中易形成阴
阴
(填“阳”或“阴”)离子(4)B粒子与Mg2+形成的化合物的化学式是
MgCl2
MgCl2
.分析:在原子中质子数等于核外电子数.质子数决定元素的种类.最外层电子数决定元素的化学性质.最外层电子数相同时,元素化学性质相似.
解答:解:(1)因D中有18个质子,所以其原子核外也应有18个电子,所以X等于8;
(2)B、C两微粒具有相同的质子数,所以两者属于同一种元素;
(3)最外层电子数决定元素的化学性质,A与B原子的最外层电子数相同,化学性质相似,在化学反应中易得到电子变成阴离子;
(4)由B粒子的原子结构示意图可知该原子是17号元素氯元素,其原子的最外层电子数为7,易得到1个电子达到稳定结构,化合价为-1价;已知镁元素的化合价为+2价,所以B粒子与Mg2+形成化合物的化学式为MgCl2;
故答案为:
(1)8;
(2)BC;具有相同的质子数(或核电荷数);
(3)A和B;阴;
(4)MgCl2
(2)B、C两微粒具有相同的质子数,所以两者属于同一种元素;
(3)最外层电子数决定元素的化学性质,A与B原子的最外层电子数相同,化学性质相似,在化学反应中易得到电子变成阴离子;
(4)由B粒子的原子结构示意图可知该原子是17号元素氯元素,其原子的最外层电子数为7,易得到1个电子达到稳定结构,化合价为-1价;已知镁元素的化合价为+2价,所以B粒子与Mg2+形成化合物的化学式为MgCl2;
故答案为:
(1)8;
(2)BC;具有相同的质子数(或核电荷数);
(3)A和B;阴;
(4)MgCl2
点评:质子数决定元素的种类,最外层电子数决定元素的化学性质,依据最外层电子数可推测其得失电子的情况,并确定元素的化合价,书写物质的化学式.

练习册系列答案
相关题目





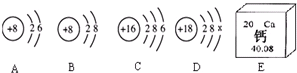 如图中A、B、C、D是四种粒子的结构示意图,E是钙元素在元素周期表中的信息.请回答下列问题:(填序号)
如图中A、B、C、D是四种粒子的结构示意图,E是钙元素在元素周期表中的信息.请回答下列问题:(填序号)