题目内容
18.NaNO2(亚硝酸钠)、NaCl 和物质M(不含结晶水)的溶解度曲线如图①所示,请根据图象和有关信息回答下列问题: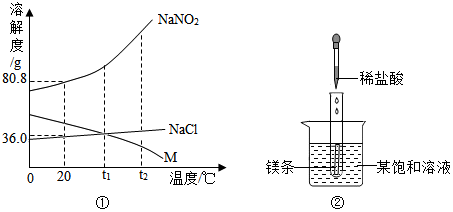
(1)t2℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是NaNO2>NaCl>M.
如图②所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).
请判断:该饱和溶液中的溶质是NaNO2、NaCl 和M 中的M.
(2)分别将NaNO2、NaCl 和M 的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质质量分数由大到小的顺序是NaNO2>NaCl>M;
(3)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故.为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息:NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃.
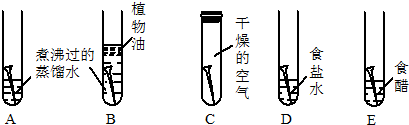
①小明同学设计的鉴别实验方案如下:20℃时分别取NaNO2、NaCl5.0g于两只小烧杯中,分别加入8mL水(水的密度近似看做1g/cm3),用玻璃棒充分搅拌后观察.你认为此方案是否可行可行.
②该小组其他同学又设计出与小明不同的实验方案,并获得成功.你认为该方案可能是:分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl(分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)由三物质的溶解度曲线可知,在t2℃时,三物质的溶解度大小关系是NaNO2>NaCl>M;
镁与稀盐酸反应放出大量的热,由题意可知,升温时该物质的饱和溶液中出现浑浊,说明该物质的溶解度随温度的升高而减小,故该饱和溶液中的溶质是M;
(2)在t2℃时,三物质的溶解度大小关系为:NaNO2>NaCl>M,因此三物质的饱和溶液中溶质的质量分数大小关系为:NaNO2>NaCl>M,当降温至t1℃时,由于NaNO2和NaCl的溶解度随温度的降低而减小,因此它们的饱和溶液中就会有晶体析出,但溶液仍旧是饱和溶液,由于在t1℃时,NaNO2比NaCl的溶解度大,因此降温以后的溶液中溶质的质量分数大小关系是NaNO2>NaCl;但由于M的溶解度随温度的降低而增大,因此降温时,M的饱和溶液就会变成不饱和溶液,但溶质的质量分数不变,虽然在t1℃时,NaCl和M的溶解度相等,但由于M已是不饱和溶液,因此溶液中溶质的质量分数大小关系是NaCl>M;
(3)20℃时,NaNO2、NaCl的溶解度分别为80.8g和36g,故向10ml水中加入5g两种物质,能全部溶解NaNO2;不能全部溶解是氯化钠;故方案可行.还可以选用分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl(或分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl).
故答案为:(1)NaNO2>NaCl>M,M;
(2)NaNO2>NaCl>M;
(3)①可行;
②分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl(分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl).
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

下列实验方案,其中可行的是( )
| A. | Zn+HCl Cu+HCl Zn+AgNO3 | |
| B. | Zn+HCl Zn+AgNO3 Cu+AgNO3 | |
| C. | Cu+HCl Zn+AgNO3 Cu+AgNO3 | |
| D. | Zn+HCl Cu+HCl Cu+AgNO3 |
| A. | 铁丝在氧气中燃烧:银白色固体燃烧,产生红色火焰,火星四射,放热,生成黑色固体 | |
| B. | 向滴有酚酞溶液的氢氧化钠溶液中通入足量二氧化碳后:溶液由红色变为无色 | |
| C. | 镁条在空气中燃烧:发出耀眼的白光,产生白烟,放热 | |
| D. | 铜丝放入硝酸银溶液中:紫红色固体表面覆盖一层银白色的银,溶液由无色变为蓝色 |