题目内容
1.同学们在完成铁与硫酸铜反应的实验后,欲从废液(含硫酸铜和硫酸亚铁)中回收金属铜,并得到硫酸亚铁,其设计的流程如下: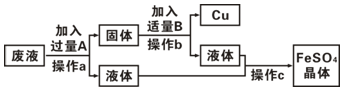
(1)操作a的名称是过滤.
(2)操作a、b和c中都需要用到的玻璃仪器是玻璃棒,其在操作c中的作用是搅拌,防止局部过热导致液滴飞溅.
(3)写出流程中固体的成分是Cu、Fe(写化学式),写出加入过量A时反应的化学方程式Fe+CuSO4═FeSO4+Cu.
分析 (1)操作a是过滤,通过过滤能够把固体和液体分离;
(2)玻璃棒的用途有搅拌、引流、转移物质等;
(3)铁能和硫酸铜反应生成硫酸亚铁和铜,能和稀硫酸反应生成硫酸亚铁和氢气.
解答 解:(1)操作a的名称是过滤,通过过滤把反应生成的铜和过量的铁与液体分离.
故填:过滤.
(2)操作a、b和c分别是过滤、搅拌和蒸发,其中都需要用到的玻璃仪器是玻璃棒,其在操作c中的作用是搅拌,防止局部过热导致液滴飞溅.
故填:玻璃棒;搅拌,防止局部过热导致液滴飞溅.
(3)流程中固体的成分是反应生成的铜和过量的铁;
加入的A是铁,铁和硫酸铜反应生成硫酸亚铁和铜,发运单号方程式为:Fe+CuSO4═FeSO4+Cu.
故填:Cu、Fe;Fe+CuSO4═FeSO4+Cu.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
11.某化学小组同学用如图甲所示的玻璃管进行碳还原氧化铜的实验.

(1)当B处的澄清石灰水变浑浊时,可观察到A处的现象是黑色粉末变成红色物质.
(2)该小组的同学通过查阅资料得知:反应生成的固体中除了铜以外还可能含有氧化亚铜(Cu2O),且氧化亚铜可以与稀硫酸发生如下反应:Cu2O+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+CuSO4+H2O.请你用学过的知识设计实验证明生成的固体全部是铜.
(3)在装置乙中,a为铁架台;图甲和图乙所示的装置相比,图甲所示的装置具有的优点是:节约药品,操作简单.(一条即可)

(1)当B处的澄清石灰水变浑浊时,可观察到A处的现象是黑色粉末变成红色物质.
(2)该小组的同学通过查阅资料得知:反应生成的固体中除了铜以外还可能含有氧化亚铜(Cu2O),且氧化亚铜可以与稀硫酸发生如下反应:Cu2O+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+CuSO4+H2O.请你用学过的知识设计实验证明生成的固体全部是铜.
| 实验操作 | 实验现象 | 实验结论 |
| 生成的固体全部是铜 |
16.对下列化学用语中数字“2”的说法正确的是( )
①2O3 ②2N ③N2 ④2NO3- ⑤Mg2+ ⑥$\stackrel{+2}{Zn}$SO4 ⑦H2O.
①2O3 ②2N ③N2 ④2NO3- ⑤Mg2+ ⑥$\stackrel{+2}{Zn}$SO4 ⑦H2O.
| A. | 表示离子个数的是④⑤ | B. | 表示离子所带电荷数的是⑤⑥ | ||
| C. | 表示分子中原子个数的是③⑦ | D. | 表示分子个数的是①② |
10.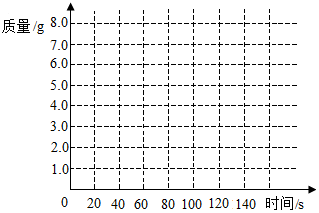 学校实验室刚刚购入了一批大理石,化学兴趣小组通过实验测定这种大理石中碳酸钙的含量.将过量的稀盐酸加入到20g大理石中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
学校实验室刚刚购入了一批大理石,化学兴趣小组通过实验测定这种大理石中碳酸钙的含量.将过量的稀盐酸加入到20g大理石中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
试回答下列问题:
(1)请在坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;
(2)从表中可以看出,20g大理石样品与盐酸反应最多能生成的CO26.6g;写出NaOH溶液吸收CO2气体的化学方程式2NaOH+CO2═Na2CO3+H2O.
(3)假如这种大理石中其他成分不与盐酸反应,计算大理石样品中碳酸钙的质量分数.
 学校实验室刚刚购入了一批大理石,化学兴趣小组通过实验测定这种大理石中碳酸钙的含量.将过量的稀盐酸加入到20g大理石中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
学校实验室刚刚购入了一批大理石,化学兴趣小组通过实验测定这种大理石中碳酸钙的含量.将过量的稀盐酸加入到20g大理石中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | 6.6 | 6.6 |
(1)请在坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;
(2)从表中可以看出,20g大理石样品与盐酸反应最多能生成的CO26.6g;写出NaOH溶液吸收CO2气体的化学方程式2NaOH+CO2═Na2CO3+H2O.
(3)假如这种大理石中其他成分不与盐酸反应,计算大理石样品中碳酸钙的质量分数.
 (1)实验中生成沉淀的质量为10g;
(1)实验中生成沉淀的质量为10g;