题目内容
9.某学校的化学兴趣小组为测定空气中S02的含量,用NaOH溶液吸收S02,反应的化学方程式为:2NaOH+SO2═Na2SO3+H2O2,用NaOH溶液吸收1000L已除去CO2的空气样品,溶液质量增加了0.64g(已知此时空气的密度约为1.3g/L).求:(1)被吸收的SO2的质量.
(2)发生反应的NaOH的质量.
(3)空气中SO2的质量分数.(计算结果精确到0.01%)
分析 (1)氢氧化钠与二氧化硫反应,溶液质量增重为二氧化硫的质量;
(2)根据方程式中质量定比关系计算NaOH的质量;
(3)根据m=ρV计算空气的质量,进而计算空气中SO2的质量分数.
解答 解:(1)氢氧化钠与二氧化硫反应,溶液质量增重为二氧化硫的质量,溶液质量增重了0.64g,即被吸收的SO2质量为0.64g,
答:被吸收的SO2质量为0.64g.
(2)设发生反应的NaOH的质量为x,
则:2NaOH+SO2═Na2SO3+H2O2
80 64
x 0.64g
$\frac{80}{x}=\frac{64}{0.64g}$
x=0.8g
答:发生反应的NaOH的质量为0.8g.
(3)空气的密度约为1.3g/L,二氧化硫质量为0.64g,
则:空气中SO2的质量分数:$\frac{0.64g}{1000L×1.3g/L}$×100%=0.05%,
答:空气中SO2的质量分数为0.05%.
点评 本题考查化学方程式有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
19.下列有关物质用途的叙述中,不正确的是( )
| A. | 氧气用于填充食品包装 | B. | 氧气用于急救病人 | ||
| C. | 氮气可用作保护气 | D. | 稀有气体可制成多种用途的电光源 |
20.现有①液态氧;②空气;③石灰水;④冰水;⑤高锰酸钾;⑥石灰石.对物质的分类全部正确的是( )
| A. | 混合物:②③⑥ | B. | 纯净物:④⑤⑥ | C. | 单质:①④ | D. | 化合物:③⑤ |
17.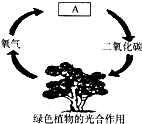 CO2在大气中含量较少,仅占空气体积的0.03%,正常情况下这一含量基本维持不变.因为在自然界中存在如下图所示的循环过程,A处不包括下列中的( )
CO2在大气中含量较少,仅占空气体积的0.03%,正常情况下这一含量基本维持不变.因为在自然界中存在如下图所示的循环过程,A处不包括下列中的( )
 CO2在大气中含量较少,仅占空气体积的0.03%,正常情况下这一含量基本维持不变.因为在自然界中存在如下图所示的循环过程,A处不包括下列中的( )
CO2在大气中含量较少,仅占空气体积的0.03%,正常情况下这一含量基本维持不变.因为在自然界中存在如下图所示的循环过程,A处不包括下列中的( )| A. | 动植物的呼吸作用 | B. | 化石燃料的燃烧 | ||
| C. | 氢气的燃烧 | D. | 酒精的燃烧 |
1.2009年6月13日是我国第四个“文化遗产日”.以下是我省部分非物质文化遗产,其制作过程主要属于物理变化的是( )
| A. | 用玉石雕琢成扬州玉雕 | B. | 用糯米酿制镇江恒顺香醋 | ||
| C. | 用紫砂泥烧制宜兴紫砂壶 | D. | 用大米和茅山泉水酿制金坛封缸酒 |
18.逻辑推理是化学学习中常用的思维方法,以下推理正确的是( )
| A. | 化合物都是由不同种元素组成的,不同元素组成的纯净物一定是化合物 | |
| B. | 碱中都有氢、氧元素,所以含氢、氧元素的化合物都是碱 | |
| C. | 中和反应有盐和水生成,生成盐和水的反应都属于中和反应 | |
| D. | 氧化物中一定含有氧元素,则另一种元素一定是金属元素 |
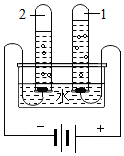 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: