题目内容
13.将一种无味的液体A装入试管,用带火星的木条试验,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C、瓶底有少量水的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F.①写出它们的名称
B:二氧化锰 C:氧气 F:四氧化三铁
②液体A遇黑色粉末B发生反应的符号表达式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 将一种无味的液体A装入试管,用带火星的木条试验,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,说明C能支持燃烧;使金属E红热并伸入盛有气体C、瓶底有少量水的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F;由过氧化氢溶液常温下分解产生氧气的速率较慢,在二氧化锰的催化作用下迅速分解生成水和氧气,铁在氧气中剧烈燃烧,火星四射,生成黑色固体四氧化三铁,进行分析解答.
解答 解:将一种无味的液体A装入试管,用带火星的木条试验,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,说明C能支持燃烧;使金属E红热并伸入盛有气体C、瓶底有少量水的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F;由过氧化氢溶液常温下分解产生氧气的速率较慢,在二氧化锰的催化作用下迅速分解生成水和氧气,铁在氧气中剧烈燃烧,火星四射,生成黑色固体四氧化三铁,则A为过氧化氢,B为二氧化锰,C为氧气,E为铁,F为四氧化三铁.
①BCF的名称分别是二氧化锰、氧气、四氧化三铁.
②液体A遇黑色粉末B,即过氧化氢在二氧化锰的催化作用下迅速分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故答案为:①二氧化锰、氧气、四氧化三铁;②2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
1.下列仪器中可直接加热的是( )
| A. | 试管 | B. | 集气瓶 | C. | 烧杯 | D. | 量筒 |
2.下列关于维生素C(C6H8O6)的说法中,正确的是( )
| A. | 维生素C是一种氧化物 | B. | 维生索C中含有4个氢分子 | ||
| C. | 维生索C的相对分子质量是176g | D. | 维生素C由碳、氢、氧三种元素组成 |
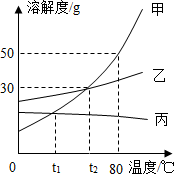 甲、乙、丙三种固体物质的溶解度曲线如图所示.据图回答问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示.据图回答问题: