题目内容
4.一定温度下,一定质量的氢氧化钠固体溶于水制成溶液.下列有关的量不随水的质量改变而改变的是( )| A. | 溶液质量分数 | B. | 溶液的pH | ||
| C. | 氢氧化钠的溶解度 | D. | 最多能吸收二氧化碳的质量 |
分析 根据已有的氢氧化钠溶于水的过程中量的变化进行分析解答即可.
解答 解;A、一定温度下,一定质量的氢氧化钠固体溶于水制成溶液,水的量越多,则溶质质量分数越小;
B、一定温度下,一定质量的氢氧化钠固体溶于水制成溶液,水的量越多,溶液的碱性越弱,则pH越小,越接近7;
C、一定温度下,一定质量的氢氧化钠固体溶于水制成溶液,氢氧化钠的溶解度不会改变;
D、一定温度下,一定质量的氢氧化钠固体溶于水制成溶液,由于二氧化碳也能溶于水,故水的量越多,吸收的二氧化碳的量也越多;
故选C.
点评 本题考查的是常见的碱氢氧化钠的性质,完成此题,可以依据已有的氢氧化钠的性质结合题干叙述进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量见表,下列税说法正确的是( )
| 物质 | a | b | c | d |
| 反应前物质质量/g | 18 | 1 | 2 | 32 |
| 反应后物质质量/g | 待测 | 26 | 2 | 12 |
| A. | 待测数据是23 | B. | 参加反应a、d的质量比为4:1 | ||
| C. | 该反应的基本类型为化合反应 | D. | c物质一定是该反应的催化剂 |
15.下列有关溶液的叙述中正确的是( )
| A. | 一种溶液中只能含一种溶质 | |
| B. | 95ml酒精和5ml水混合后溶剂是酒精 | |
| C. | 溶液是一种均一、稳定的混合物 | |
| D. | 溶液中的溶成质一定是固体,溶剂一定是水 |
19.下列说法正确的是( )
| A. | 饱和溶液析出晶体后,溶质的质量分数一定减少 | |
| B. | 常温下KNO3、Ca(OH)2的饱和溶液降温后仍是饱和溶液 | |
| C. | 将NaCl、蔗糖溶于水后,溶质均以分子形式存在 | |
| D. | 20℃时100g10%的氯化钠溶液中,氯化钠与水的质量比为1:9 |
13.下列变化中,属于物理变化的是( )
| A. | 电解水 | B. | 干冰气化 | C. | 铁生锈 | D. | 白磷自燃 |
 钢铁在生产生活中具有广泛用途.
钢铁在生产生活中具有广泛用途.
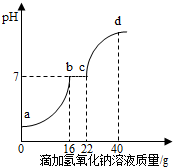 为测定某工业盐酸中氯化铁的含量(假设工业盐酸中不含其它杂质),小娟做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为20%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如右图所示的关系.
为测定某工业盐酸中氯化铁的含量(假设工业盐酸中不含其它杂质),小娟做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为20%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如右图所示的关系.