题目内容
根据下图所示的实验装置图回答:
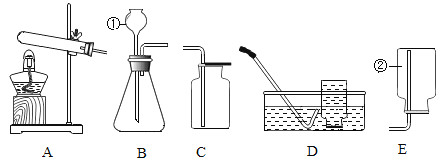
(1)写出编号的仪器名称:①_____;②_____;
(2)实验室常用稀盐酸和石灰石反应制取CO2,该反应的化学方程式为:_____;制取并收集CO2,应选用的装置为_____(填序号)。
(3)如果要检验二氧化碳是否收集满,可将_____。
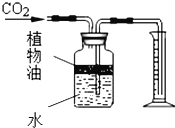
(4)如图所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是:_____,植物油上方原有空气对实验结果_____(填“有”或“无”)明显影响.
(5)在加热氯酸钾和二氧化锰混合物制氧气实验中,混合物总质量100g,反应一段时间后,二氧化锰的质量分数由20%变为25%求氯酸钾的分解率。_____。(提示:分解率是分解的质量比原质量)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0g石灰石样品,把25.0g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0g |
剩余固体的质量 | 1.5g | m | 0.5g | 0.3g | 0.3g |
计算:
(1)m=______g。
(2)石灰石中碳酸钙的质量分数为______。
(3)2.0g石灰石样品与足量稀盐酸反应,产生二氧化碳的质量是多少?_____(写出解题过程)
实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小明用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如表,请分析计算(写出计算过程)
实验组别 | 一 | 二 | 三 | 四 |
稀盐酸质量/g | 100.0 | 100.0 | 100.0 | 100.0 |
混合物质量/g | 3.0 | 6.0 | 9.0 | 12.0 |
所得溶液质量/g | 101.9 | 103.8 | 105.0 | a |
剩余固体质量/g | 0 | 0 | m | n |
(1)求混合物中碳酸钙和氯化钙质量之比__________
(2)表中a的值为_______。
(3)求表中m的值__________。



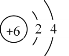 ,碳原子的核电荷数为_______。
,碳原子的核电荷数为_______。 B
B  C
C