题目内容
5. 小东同学用如图所示气密性良好的装置进行有关实验.图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,其左端密封有空气和足量白磷(白磷着火点40℃,红磷的着火点240℃)和红磷,右端跟空气相通,实验开始前,活塞处在5cm处.
小东同学用如图所示气密性良好的装置进行有关实验.图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,其左端密封有空气和足量白磷(白磷着火点40℃,红磷的着火点240℃)和红磷,右端跟空气相通,实验开始前,活塞处在5cm处.(1)实验开始时,可以观察到玻璃管内红磷不燃烧,(填燃烧或不燃烧)原因是温度没有达到着火点.实验结束后,恢复至常温,活塞应停在约4cm处,据此可得出关于空气组成的结论是空气中氧气约占$\frac{1}{5}$体积.
(2)实验完毕,小东将烧杯中的热水慢慢倒出,水快倒完时,白磷刚露出水面就燃烧起来.请分析产生该现象的原因白磷的温度达到着火点,露出水面后又与氧气接触,因此白磷燃烧.说明可燃物燃烧需要满足的条件是可燃物与氧气接触、温度达到着火点.
(3)请写出磷燃烧的符号表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
分析 (1)根据白磷着火点低,热水可使它达到着火点,玻璃管内的白磷满足燃烧的条件.其他都不满足燃烧的条件.白磷的燃烧需要消耗氧气,氧气的体积占空气体积的$\frac{1}{5}$,使玻璃管内的压强变小,活塞向左移动进行分析;
(2)根据烧杯中的白磷能够燃烧是因为与氧气接触进行分析;
(3)根据反应物和反应条件以及生成物写出化学反应式.
解答 解:(1)据题意可知,白磷的着火点是40℃,红磷的是240℃.玻璃管内有充足的空气,烧杯内的热水可使白磷的达到着火点,所以白磷燃烧,红磷不燃烧.白磷的燃烧消耗氧气,是玻璃管内的压强变小,在外界大气压的作用下活塞向下左移动.又因为氧气的体积占空气体积的$\frac{1}{5}$,所以活塞移到4cm处;
(2)烧杯内的白磷开始时不能燃烧是因为没有与空气接触,当水倒出时,白磷与空气充分接触,使白磷燃烧.据此可知与空气或氧气接触是可燃物的燃烧的条件之一;
(3)根据反应物是磷和氧气、反应条件是点燃、生成物是五氧化二磷,化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故答案为:(1)不燃烧,温度没有达到着火点,4,空气中氧气约占$\frac{1}{5}$体积;
(2)白磷的温度达到着火点,露出水面后又与氧气接触,因此白磷燃烧;可燃物与氧气接触;
(3)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
点评 本题考查物质燃烧的条件以及氧气的体积和化学方程式的书写.使学生巩固了基础知识.

练习册系列答案
相关题目
20. 如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法错误的是( )
如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法错误的是( )
 如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法错误的是( )
如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法错误的是( )| A. | 化学变化过程中一定有新物质的分子生成 | |
| B. | 化学反应前后原子的种类不变 | |
| C. | 该反应类型为分解反应 | |
| D. | 该反应的反应物是混合物 |
17.根据实验操作所绘制的图象中,正确的是( )
| A. |  将铁粉加入到一定量的稀盐酸中,生成氢气的质量与加入铁粉的质量关系 | |
| B. | 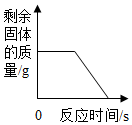 用加热一定量的高锰酸钾,剩余固体质量与反应时间的关系 | |
| C. |  向等质量的金属镁和铝中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系 | |
| D. |  向氢氧化钠、氢氧化钡混合溶液中加入硫酸,生成沉淀的质量和加入硫酸质量的关系 |
14.物质的下列性质中,属于化学性质的是( )
| A. | 颜色、状态 | B. | 氧化性、可燃性 | C. | 密度、硬度 | D. | 熔点、沸点 |


 化合反应和氧化反应的关系可用如图表示,
化合反应和氧化反应的关系可用如图表示,
