题目内容
4.为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,小军取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分4次加入烧杯中,均充分反应,实验数据如下:| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.10 | 8.45 | 7.80 | 7.80 |
(2)所用稀盐酸中溶质的质量分数为7.3%;
(3)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为8g;
(4)黄铜样品中铜的质量分数为多少?
分析 (1)根据金属活动性可知,铜排在氢后,不能与稀盐酸发生反应,故发生反应的是锌,减少的固体的质量就是参加反应的锌的质量,由题目可知:第二次反应消耗锌的质量=9.10g-8.45g=0.65g;
(2)利用第二次实验所消耗锌的量,根据反应的化学方程式,计算出所加10g稀盐酸中溶质的质量,由溶质的质量分数公式,求出所用稀盐酸中溶质的质量分数;
(4)根据加水稀释前后溶液中溶质质量不变,由40g7.3%的稀盐酸中溶质质量与浓盐酸的质量分数的比计算需要浓盐酸的质量;
(5)根据第四次实验数据可知,剩余的7.80g固体即为样品中铜的质量,铜的质量与样品质量比可计算出黄铜样品中铜的质量分数,而样品的质量=9.10g+0.65g=9.75g.
解答 解:(1)Zn的质量=0.65g×3=1.95g
Zn-----H2↑
65 2
1.95g 0.6g
所以生成氢气是0.6g;
(2)设10g稀盐酸中HCl的质量为y
Zn+2HCl═ZnCl2+H2↑
65 73
0.65g y
$\frac{65}{0.65g}$=$\frac{73}{y}$
y=0.73g
所用稀盐酸中溶质的质量分数=$\frac{0.73g}{10g}$×100%=7.3%
(3)需要浓盐酸的质量=$\frac{40g×7.3%}{36.5%}$=8g
(4)由第二次实验可知,第一次加入10g稀盐酸时,反应消耗锌的质量为0.65g,则原黄铜样品的质量=9.10g+0.65g=9.75g;由第四次实验可知,样品中铜的质量7.8g
黄铜样品中铜的质量分数=$\frac{7.8g}{9.75g}$×100%=80%.
故答案为:(1)0.6;
(2)7.3%;
(3)8g;
(4)80%.
点评 分析每次加入10g稀盐酸固体剩余物质量的变化,可对反应进行的情况进行判断,这是解决本题的基础.

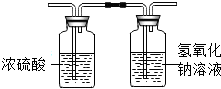 某气体由H2、CO、CH4中的一种或几种组成,点燃该气体后,将所得气体依次通过如图装置,测得两装置的质量均增加,则下列对该气体成分的推断不正确的是( )
某气体由H2、CO、CH4中的一种或几种组成,点燃该气体后,将所得气体依次通过如图装置,测得两装置的质量均增加,则下列对该气体成分的推断不正确的是( )| A. | 可能只有CH4 | B. | 可能只有H2 | ||
| C. | 可能是CO和CH4 | D. | 可能三种气体都存在 |
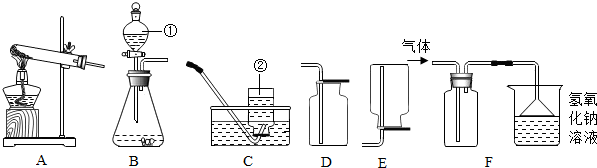
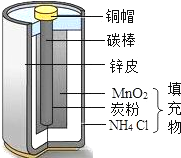
(1)图1所示用品中,利用金属导电性的是B(填字母序号).
(2)下表是一些金属的熔点数据.

| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
(3)新型材料纳米级Fe粉在空气中易自燃,能用作高效催化剂,实验室采用还原法制备纳米级Fe粉,流程如图3:
①铁丝在空气中只能灼成红热、离火变冷,而纳米级Fe粉在空气中易自燃,说明物质燃烧的剧烈程度与药品的状态(可燃物与氧气的接触面积)有关.
②写出Ⅱ中用氢气从FeCl2置换出铁的反应方程式H2+FeCl2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl.
在Ⅱ中通入氮气的目的是排尽空气,防止生成的铁粉被反应.
(4)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较强的金属首先被腐蚀.造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是D.(填编号)
A、银块 B、铜块 C、锡块 D、锌块
(5)用下列试剂探究不同金属与酸反应的速率不同:锌片、铁片、5%盐酸.取质量相等的上述两种金属(表面积相同),分别放入溶质质量分数5%的足量稀盐酸中.
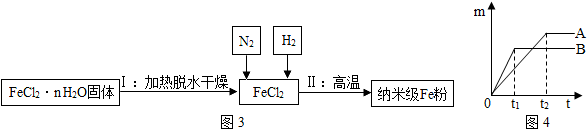
①线B对应的金属是Zn.
②线A对应的金属与稀盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑.
(6)某兴趣小组的同学将一块不纯的铁片5.6g投入到足量的稀盐酸中,充分反应后生成了0.2g气体,则该铁片中混有的杂质一定不可能是D.
A、铝和锌 B、镁和锌 C、镁和铜 D、锌和铜.
| A. | 生石灰、烧碱、浓硫酸都可以用作干燥剂 | |
| B. | 铁、锌、碘元素都属于人体必需微量元素 | |
| C. | CH4、C2H5OH、CH3COOH 都属于有机化合物 | |
| D. | KNO3、CO(NH2)2、NH4H2PO4 都属于复合肥料 |
| A. | 电子数 | B. | 质子数 | C. | 中子数 | D. | 最外层电子数 |
| A. | 随地焚烧垃圾 | B. | 多植树造林 | ||
| C. | 多使用含磷洗衣粉 | D. | 随地吐痰 |
 生活中处处有化学.
生活中处处有化学.