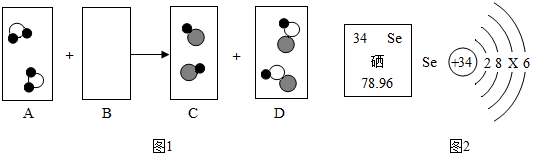
题目内容
6.为了除去下列物质中的杂质(括号内是杂质),下列操作方法中,正确的是( )| 选项 | 物质 | 操作方法 |
| A | Fe (Fe2O3) | 加入过量稀盐酸,充分反应后过滤 |
| B | CaO粉末(CaCO3粉末) | 加足量的水,充分搅拌后过滤 |
| C | CuSO4 (H2SO4) | 加入足量的NaOH溶液,充分反应后过滤 |
| D | NaOH溶液(Na2CO3) | 加入适量Ca(OH)2溶液,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Fe和Fe2O3均能与盐酸溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、H2SO4和CuSO4均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、Na2CO3能与适量Ca(OH)2溶液反应生成碳酸钙沉淀和氢氧化钠,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.2012年9月20日西溪湿地第六届火柿节开幕了,欢乐的“柿民们”纷纷采摘柿子来吃,却发现有些柿子很涩,这是因为柿子中含有一种物质叫鞣酸( C76H52O46).下列有关鞣酸的说法中,正确的是( )
| A. | 鞣酸不属于氧化物,属于有机物 | |
| B. | 鞣酸溶液能使无色酚酞变红 | |
| C. | 鞣酸中C、H、O元素质量比为38:26:23 | |
| D. | 鞣酸溶液能使红色石蕊试纸变蓝 |
11.据有关新闻媒体报道:经抽检发现燕窝市场中“血燕”的亚硝酸盐含量严重超标,最高超标350倍.亚硝酸钠外观酷似食盐且有咸味,如果将亚硝酸钠(NaNO2)误作食盐食用或摄入过量亚硝酸钠后,可引起中毒,甚至死亡.根据亚硝酸钠的化学式可确定它的NO2-(请填写组成成分的化学符号)是有毒的;请设计一个实验来鉴别食盐和亚硝酸钠,在表中填写相关操作步骤、现象和结论.
| 操作步骤 | 现象和结论 |
| 分别取少量待测固体于试管中,加入适量的水溶解,分别滴加几滴硝酸银溶液 | 产生白色沉淀的原固体是氯化钠,无明显变化的是原固体是亚硝酸钠 |
18.“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺,同学们查阅相关资料并进行模拟实验.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:
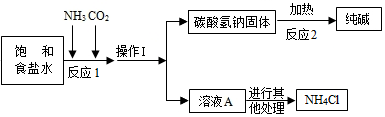
③氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度NH4Cl的溶解度<(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
【实验反思】同学们认为步骤3的结论存在不足.依据题中信息,设计实验确定步骤2加热后得到的固体成分,其方案是将生成的气体通入澄清的石灰水,观察到澄清的石灰水变浑浊,证明步骤2加热后得到的是碳酸氢钠.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:

③氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
(1)依据资料①可知相同条件下,NaHCO3的溶解度NH4Cl的溶解度<(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
【模拟实验】验证侯氏制碱法能获得纯碱
| 步骤 | 蘸有稀硫酸 实验装置 | 实验操作及现象 | 解释与结论 |
| 1 | 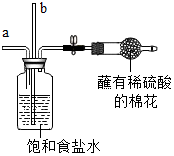 | 从a管通入NH3,一段时间后,从b管通入CO2,溶液中有固体析出 | (1)蘸有稀硫酸的棉花的作用是 (2)通NH3的a管若伸到液面下,会造成的后果是 |
| 2 | 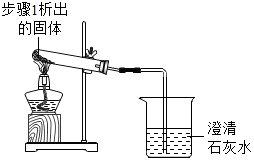 | 加热,导管口有气泡,澄清石灰水变浑浊 | 步骤1析出的固体是碳酸氢钠 |
| 3 | 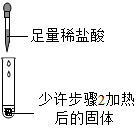 | 滴加足量稀盐酸,有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
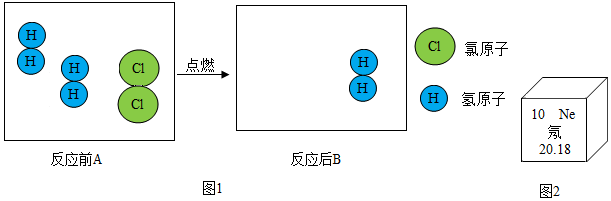
 ”表示氯原子,用“
”表示氯原子,用“ ”
”