题目内容
a g KClO3与b g MnO2混合后,充分加热,得剩余固体c g,则生成O2的质量为 ,KCl的质量为 .
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,据此结合质量守恒定律,反应前后物质的总质量不变,进行分析解答.
解答:解:氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,agKClO3与b g MnO2混合后,充分加热,得剩余固体cg,有质量守恒定律,则生成O2的质量为ag+bg-cg=(a+b-c)g;剩余固体为氯化钾和二氧化锰的混合物,则生成氯化钾的质量为cg-bg=(c-b)g.
故答案为:(a+b-c)g;(c-b)g.
故答案为:(a+b-c)g;(c-b)g.
点评:本题难度不大,掌握质量守恒定律、氯酸钾分解制取氧气的反应原理并能灵活运用是正确解答本题的关键.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
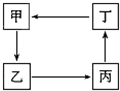 甲、乙、丙、丁四种物质有如图所示的转化关系(“→”表示物质间存在转化关系,部分反应物和产物已略去),则甲、乙、丙、丁依次是( )
甲、乙、丙、丁四种物质有如图所示的转化关系(“→”表示物质间存在转化关系,部分反应物和产物已略去),则甲、乙、丙、丁依次是( )| A、CO2、Ca(OH)2、CaCO3、HCl |
| B、H2O、O2、CO2、H2CO3 |
| C、CO、CO2、CaCO3、HCl |
| D、C、CO、CO2、H2CO3 |
取用100g铁粉和100g镁粉分别和相同浓度的稀硫酸发生反应,通过计算进行比较:
(1)如果两种金属盒酸反应生成等质量的气体,消耗何种金属最多?
(2)如果铁粉和镁粉都反应完,消耗稀硫酸最多的是何种金属?
(1)如果两种金属盒酸反应生成等质量的气体,消耗何种金属最多?
(2)如果铁粉和镁粉都反应完,消耗稀硫酸最多的是何种金属?
下列物质中既不存在分子又不存在离子的是( )
| A、氯化钠晶体 | B、水 |
| C、氢氧化钠溶液 | D、金刚石 |
根据如图所示的溶解度曲线,判断下列说法正确的是( )
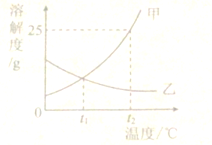

| A、t1℃时,甲、乙两种溶液的溶质质量分数一定相等 |
| B、t1℃时,甲、乙两种物质的饱和溶液中含溶质的质量相等 |
| C、t1℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等 |
| D、乙物质的饱和溶液从t2℃降温到t1℃,其溶质的质量分数减少 |