题目内容
20.乙醇是一种清洁燃料,但在氧气不足时燃烧,会生成一氧化碳.现有276g乙醇与一定量的氧气点燃后发生如下反应:3C2H5OH+8O2$\frac{\underline{\;点燃\;}}{\;}$XCO2+2CO+9H2O(1)若该化学方程式已配平,则X=4;
(2)计算该反应生成的一氧化碳的质量.(写出计算过程)
分析 (1)根据质量守恒定律,反应前后碳原子个数不变,进行分析解答.
(2)由参加反应的乙醇的质量,由反应的化学方程式列式计算出生成一氧化碳的质量即可.
解答 解:(1)由质量守恒定律,反应前后碳原子个数不变,则3×2=x+2×1,x=4.
(2)设该反应生成的一氧化碳的质量为x
3C2H5OH+8O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2CO+9H2O
138 56
276g x
$\frac{138}{56}=\frac{276g}{x}$ x=112g
答:(1)4;(2)该反应生成的一氧化碳的质量为112g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出x的值是正确解答本题的前提和关键.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
10.科研人员调查发现,人的某些心血管疾病,如高血压和动脉硬化性心脏病的死亡率,与饮水的硬度成反比,水质硬度低,死亡率反而高,长期饮用过硬或者过软的水都不利于人体健康.下列说法中正确的是( )
| A. | 硬水比软水洗衣服的效果好 | B. | 硬水中含较多钙离子和镁离子 | ||
| C. | 硬水放一段时间就变成软水 | D. | 凡是含有杂质的水就是硬水 |
15.通过实验测定了空气的组成的科字家是( )
| A. | 门捷列夫 | B. | 道尔顿 | C. | 拉瓦锡 | D. | 牛顿 |
5.实验室中要配制一定溶质质量分数的氯化钠溶液,请你帮助完成. 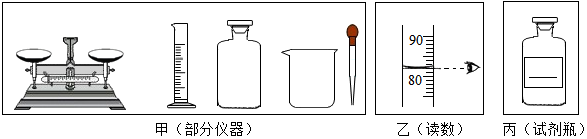
①甲图中缺少一种必须用到的玻璃仪器是玻璃棒(填写名称).
②配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、溶解、装瓶并贴上标签.

①甲图中缺少一种必须用到的玻璃仪器是玻璃棒(填写名称).
②配制氯化钠溶液的操作过程依次是:氯化钠的称量、水的量取、溶解、装瓶并贴上标签.
2.现有一包白色粉末,可能由NaCl、Na2CO3、Na2SO4、CuSO4中的一种或几种组成,现做如下实验:
反思:实验步骤(2)中能否将稀硝酸改为滴加稀盐酸或稀硫酸不能,原因是会影响氯化钠和硫酸钠的检验.
| 实验操作 | 实验现象 | 结论 |
| (1)取少量粉末,加入适量水溶解,振荡. | 粉末溶解,得到无色溶液. | 由此可知原粉末中一定没有CuSO4 |
| (2)向(1)中溶液滴入过量稀硝酸. | 产生气泡 | 可确定原粉末中一定含有Na2CO3 |
| (3)向(2)溶液中滴入过量的硝酸钡溶液 | 产生白色沉淀 | 可确定原粉末中一定含有Na2SO4 |
| (4)过滤,向滤液中加入少量的硝酸银溶液 | 没有明显现象 | 可确定原粉末中一定不含有NaCl |
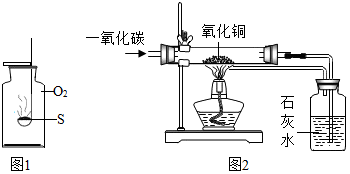 “绿色化学”强调采取有效措施,节约能源、防止对环境的破坏和污染.化学实验设计应该尽可能符合“绿色化学”的要求.
“绿色化学”强调采取有效措施,节约能源、防止对环境的破坏和污染.化学实验设计应该尽可能符合“绿色化学”的要求.