题目内容
在研究某石灰石样品(杂质不含钙也不与盐酸反应)的活动中,兴趣小组同学进行了如下实验.请根据实验过程和提供的数据(盐酸足量,且反应产生的气体全部逸出)计算该石灰石样品中碳酸钙的质量分数.
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12.5g | 158.1g | |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:反应前后烧杯及烧杯内物质的质量之差为生成的二氧化碳的质量,根据化学方程式利用二氧化碳的质量求碳酸钙的质量,进而求得其质量分数.
解答:解:根据质量守恒定律,完全反应产生CO2质量:12.5g+150g-158.1g=4.4g;
设12.5g样品中碳酸钙质量为x,
CaCO3+2HClCaCl2+H2O+CO2↑
100 44
x 4.4g
=
解得:x=10g
则样品中碳酸钙的质量分数是:
×100%=80%
答:该石灰石中碳酸钙的质量分数是为80%.
设12.5g样品中碳酸钙质量为x,
CaCO3+2HClCaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| 44 |
| x |
| 4.4g |
解得:x=10g
则样品中碳酸钙的质量分数是:
| 10g |
| 12.5g |
答:该石灰石中碳酸钙的质量分数是为80%.
点评:正确分析表格内的数据是正确解答本题的关键.

练习册系列答案
相关题目
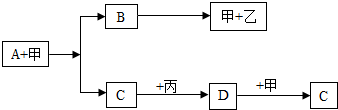
科学家正在研究如图所示的循环体系.
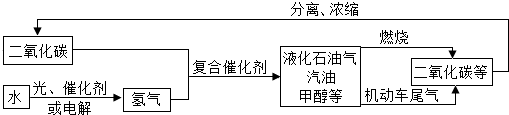
从图中分析得出的下列结论正确的是( )
①该技术符合低碳经济的理念 ②该过程所用的催化剂一定是二氧化锰
③该体系有一种可循环利用的物质是氢气 ④该技术有助于缓解全球面临的能源危机
⑤二氧化碳与氢气在复合催化剂条件下反应的产物是混合物.

从图中分析得出的下列结论正确的是( )
①该技术符合低碳经济的理念 ②该过程所用的催化剂一定是二氧化锰
③该体系有一种可循环利用的物质是氢气 ④该技术有助于缓解全球面临的能源危机
⑤二氧化碳与氢气在复合催化剂条件下反应的产物是混合物.
| A、①②④ | B、①③⑤ |
| C、②③⑤ | D、①④⑤ |
某物质在充足的氧气中燃烧、只生成CO2和H2O、且CO2和H2O的质量比为22:9、则该物质是( )
| A、C2H6 |
| B、CH4 |
| C、C3H6 |
| D、CH3OH |
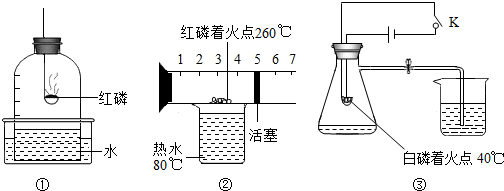
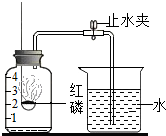 已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验:在燃烧匙内盛过量红磷,点燃后立即插入充满空气的集气瓶中,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温后,再打开止水夹.实验装置如图所示
已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验:在燃烧匙内盛过量红磷,点燃后立即插入充满空气的集气瓶中,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温后,再打开止水夹.实验装置如图所示