题目内容
11.纳米材料具有特殊的性质和功能.纳米二氧化钛(TiO2)参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度.正钛酸(H4TiO4)在一定条件下分解失水可制得纳米TiO2.下列说法正确的是( )| A. | TiO2属于非金属氧化物 | |
| B. | 纳米TiO2与普通的TiO2的性质、功能完全相同 | |
| C. | 纳米TiO2添加到墙面涂料中,可消除甲醛一定条件 | |
| D. | 制备纳米TiO2的反应:H4TiO4$\frac{\underline{\;一定条件\;}}{\;}$TiO2+H2O |
分析 A、TiO2属于金属氧化物.
B、纳米TiO2具有独特的光催化性、优异的颜色效应及紫外线屏蔽等功能.
C、二氧化钛(TiO2)可做成纳米材料,在光的催化作用下,将甲醛等有害物质降解成二氧化碳和水.
D、根据反应物与生成物,以及质量守恒定律进行分析判断.
解答 解:A、TiO2属于金属氧化物,故A错误;
B、纳米 TiO2 具有独特的光催化性、优异的颜色效应及紫外线屏蔽等功能,普通的TiO2则没有,故B错误;
C、二氧化钛(TiO2)可做成纳米材料,在光的催化作用下,将甲醛等有害物质降解成二氧化碳和水,能有效去除因装修带来的多种有害气体.故C正确;
D、正钛酸(H4TiO4)在一定条件下分解失水可制得纳米TiO2.化学方程式为:H4TiO4$\frac{\underline{\;一定条件\;}}{\;}$TiO2+2H2O,故D正确.
故选CD.
点评 本题难度不大,主要考查纳米二氧化钛的应用以及制取方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.为了除去物质中的杂质(括号内物质为杂质),不能达到除杂目的是( )
| 物质 | 选用试剂 | 操作方法 | |
| A | 氧化钙(碳酸钙) | 高温加热 | |
| B | 氮气(氧气) | 灼热的铜网 | 气体通过 |
| C | 硫酸铜溶液(硫酸) | 过量的氧化铜 | 加入氧化铜充分反应后过滤 |
| D | 氯化钠溶液(碳酸钠) | 过量氯化钙溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.元素周期表中,氟元素的信息如图所示.下列解释不正确的是( )
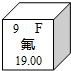

| A. | 原子序数是9 | B. | 氟是非金属元素 | ||
| C. | 质子数是19 | D. | 相对原子质量是19.00 |
19.通过实验能达到目的是( )
| A. | 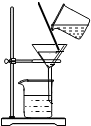 分离溶液中NaCl和CaCl2两中溶质 分离溶液中NaCl和CaCl2两中溶质 | B. | 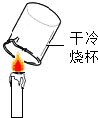 检验蜡烛燃烧生成的水 检验蜡烛燃烧生成的水 | ||
| C. |  鉴定溶液中溶质是否含有碳酸根 鉴定溶液中溶质是否含有碳酸根 | D. | 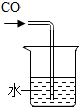 用水吸收CO 用水吸收CO |
6.红细胞的血红蛋白含有铁.这里的“铁”是指( )
| A. | 铁元素 | B. | 铁原子 | C. | 铁单质 | D. | 铁离子 |
20.下列物质的用途与其物理性质有关的是( )
| A. | 用活性炭除去冰箱异味 | B. | 用氮气作食品包装袋的填充气 | ||
| C. | 用碳素墨水写文字档案便于保存 | D. | 氧气供给呼吸 |
1.如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子.下列说法中错误的是( )


| A. | 甲、乙、丙都属于氧化物 | |
| B. | 该反应属于化合反应 | |
| C. | 反应前后,原子种类和数目均不变 | |
| D. | 反应中,甲、乙、丙三种物质的分子个数比为2:1:2 |
 随着经济的发展,能源与环境成为人们日益关注的问题.
随着经济的发展,能源与环境成为人们日益关注的问题.