题目内容
古代“银针验毒”的原理是4Ag+2H2S+X→2Ag2S+2H2O,X的化学式为( )
|
| A. | H2 | B. | S | C. | O2 | D. | SO2 |
| 质量守恒定律及其应用 | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 化学反应前后,元素的种类不变,原子的种类、总个数不变. |
| 解答: | 解:由4Ag+2H2S+X→2Ag2S+2H2O可知, 反应前银原子的相对个数是4个,反应后是4个; 反应前氢原子的相对个数是4个,反应后是4个; 反应前硫原子的相对个数是2个,反应后是2个; 反应后氧原子的相对个数是2个,反应前应该是2个,包含在X中,X是氧气,化学是O2. 故选:C. |
| 点评: | 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl(其他成分不考虑)。请回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是 。(填字母)
A.10mL B.50mL C.100mL
(2)下图是配制过程,正确的操作顺序为 。(填序号)
 |
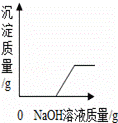
(3)为测定味精中NaCl的质量分数,进行如下实验:
①向所配制的50g溶液中加入过量的 溶液(填化学式)充分反应。
②然后进行 (填操作名称)、洗涤、干燥后称量AgCl固体。
③在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数 (填“偏大”、“偏小”或“无影响”),则测得的样品中氯化钠的质量分数 (填“偏大”、“偏小”或“无影响”)。
④经精确测定AgCl沉淀的质量为2.87g,则该味精中NaCl的质量分数为 。(计算结果保留一位小数)
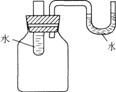
下列实验操作符合规范的是( )
|
| A. |
检验装置气密性 | B. |
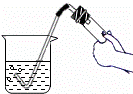
给液体加热 | C. |
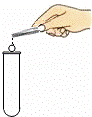
向试管中加固体 | D. |
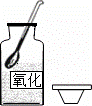
取用固体药品 |
“凤凰”号火星探测器测得火星北极的土壤呈弱碱性,如果火星具备作物生长的条件,下列作物较适宜在火星北极种植的是( )
| 植物 | 大豆 | 棉花 | 茶树 | 松树 |
| pH | 6.5﹣7.5 | 6.0﹣6.8 | 5.0﹣5.5 | 5.0﹣6.0 |
|
| A. | 大豆 | B. | 棉花 | C. | 茶树 | D. | 松树 |