题目内容
4.已知HCl、NaOH、Al(OH)3、AlCl3和NaAlO2溶液之间可以发生一系列反应,如图(纵坐标为产生沉淀物的质量/g,横坐标为加入AlCl3溶液的体积/mL)中,能够正确描述“往NaOH溶液中逐滴滴入AlCl3溶液至过量”的实验中,产生沉淀物的质量与滴加溶液体积之间的关系的是( )| A. | 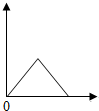 | B. | 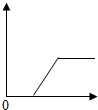 | C. |  | D. |  |
分析 由题给信息:由AlCl3+3NaOH=Al(OH)3↓+3NaCl,知NaOH和Al(OH)3反应的化学计量数比为3:1;由Al(OH)3+NaOH=NaAlO2+2H2O,知NaOH和Al(OH)3反应的化学计量数比为1:1;即推出产生白色Al(OH)3的质量与NaOH溶液的质量关系,参照选项图示既得答案.
解答 解:A、由AlCl3+3NaOH=Al(OH)3↓+3NaCl,知方程式中NaOH和Al(OH)3化学计量数比为3:1,由Al(OH)3+NaOH=NaAlO2+2H2O,知NaOH和Al(OH)3反应的化学计量数比为1:1;推断出图象A表达不准确;故A选项错误;
B、由AlCl3+3NaOH=Al(OH)3↓+3NaCl,知一开始滴加AlCl3溶液时,就有沉淀生成,而图示中需要滴加一定量的AlCl3溶液后才有沉淀生成;所以图象B表述不正确;故B选项错误;
C、由AlCl3+3NaOH=Al(OH)3↓+3NaCl,知方程式中NaOH和Al(OH)3化学计量数比为3:1,由Al(OH)3+NaOH=NaAlO2+2H2O,知NaOH和Al(OH)3反应的化学计量数比为1:1;推断出图象C表达不准确;故C选项错误;
D、由AlCl3+3NaOH=Al(OH)3↓+3NaCl,知方程式中NaOH和Al(OH)3化学计量数比为3:1,由Al(OH)3+NaOH=NaAlO2+2H2O,知NaOH和Al(OH)3反应的化学计量数比为1:1;推断出图象D表达准确;故D选项正确.
故选D.
点评 此题主要是对题意中出现的两个方程式进行分析、计算,找出量的关系比与图象结合理解即可.能考查学生的逻辑思维能力.

练习册系列答案
相关题目
18.下列说法中,正确的是( )
| A. | 分解反应就是由一种物质生成两种物质的反应 | |
| B. | 氧化反应不一定是化合反应,化合反应也不一定是氧化反应 | |
| C. | 凡是在空气中不能燃烧的物质,在纯氧中也不能燃烧 | |
| D. | 钢铁锈蚀的过程中只含化学变化 |
19.某化学兴趣小组的同学,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R;猜想二:Al>R>Cu;猜想三:R>Al>Cu;
【查阅资料】R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色;常温下R的表面会形成一层氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色.
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究.
【交流反思】究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前对铝丝打磨不够彻底,这可能会导致实验结论错误.于是他们把铝丝反复打磨后,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色变成无色,进而确认猜想三不成立,猜想二成立.
【归纳总结】探究结束后,他们总结得出:通过金属与酸反应或金属与盐溶液反应可以比较金属活动性强弱.
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R;猜想二:Al>R>Cu;猜想三:R>Al>Cu;
【查阅资料】R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色;常温下R的表面会形成一层氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色.
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究.
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一不成立(填“成立”或“不成立”) |
猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立. R与稀硫酸反应的化学方程式为 R+H2SO4=RSO4+H2↑ |
| 猜想三 | 将打磨过的铝丝,插入到RSO4溶液中 | 无明显现象 | 猜想三成立 |
【归纳总结】探究结束后,他们总结得出:通过金属与酸反应或金属与盐溶液反应可以比较金属活动性强弱.
9.现有表面被氧化的镁条样品6.4g,加入到盛有200g7.3%的稀盐酸的烧杯中,恰好完全反应.则被氧化的镁占原镁条的质量分数为( )
| A. | 50.0% | B. | 37.5% | C. | 48.1% | D. | 80.4% |

 代表碳原子
代表碳原子 代表氧原子)
代表氧原子)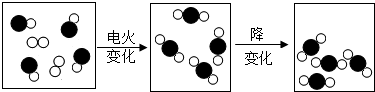
 铜钱:古代铜质辅币,俗称铜钱,黄铜在明清时期就用于铸造铜钱了,小明对铜钱(主要成分为铜和锌)中铜的质量分数产生了好奇,他称取10g铜钱样品放入烧杯中,然后往烧杯中加入稀硫酸93.5g,恰好完全反应,反应后称得烧杯内物质共103.3g.
铜钱:古代铜质辅币,俗称铜钱,黄铜在明清时期就用于铸造铜钱了,小明对铜钱(主要成分为铜和锌)中铜的质量分数产生了好奇,他称取10g铜钱样品放入烧杯中,然后往烧杯中加入稀硫酸93.5g,恰好完全反应,反应后称得烧杯内物质共103.3g.